题目内容
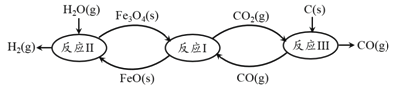
【题目】工业上炼铁的主要流程如图:
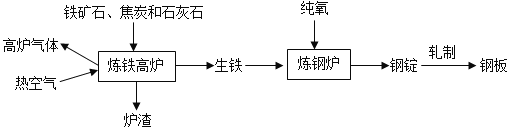
(1)流程中涉及反应有:①Fe2O3+CO![]() 2Fe+3CO2;② Fe2O3+C
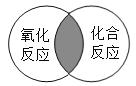
2Fe+3CO2;② Fe2O3+C![]() 2Fe+3CO用于高炉炼铁的原理是____________(填序号),反应②的反应类型是______________。
2Fe+3CO用于高炉炼铁的原理是____________(填序号),反应②的反应类型是______________。
(2)炼铁的各种固体原料需混合均匀一起加入高炉,其目的是____________________________。
(3)高炉气体的主要成分是______________。炉渣主要成分是硅酸钙(CaSiO3),其中元素Ca、Si、O的质量比是______________。
(4)从铁矿石得到单质铁其中铁的化合价______________(填升高或降低)。
(5)根据金属活动顺序表自己选择一种金属与FeSO4溶液反应得到单质铁的方程式是:_____________。
【答案】① 置换反应 增大反应物的接触面积,使其充分反应 氮气 10:7:12 降低 Zn+FeSO4=ZnSO4+Fe(合理均可)
【解析】
(1)高炉炼铁是一氧化碳还原氧化铁;一种单质和一种化合物反应生成另一种单质和另一种化合物,是置换反应。
(2)炼铁的各种固体原料需混合均匀一起加入高炉,其目的是增大反应物的接触面积,使其充分反应。
(3)高炉煤气为炼铁过程中产生的副产品,主要成分为:CO、CO2、 N2、H2、CH4 等。其中可燃成分 CO 含量约占 25%左右;H2、CH4 的含量很少;CO2、N2 的含量分别 占 15%、55 %。
(4)从铁矿石得到单质铁,铁的化合价由+3降低到0。
(5)根据金属活动顺序,可以用锌与FeSO4溶液反应得到单质铁和硫酸锌。
(1)高炉炼铁是一氧化碳还原氧化铁,原理是①,反应②的反应类型是一种单质和一种化合物反应生成另一种单质和另一种化合物,是置换反应。
(2)炼铁的各种固体原料需混合均匀一起加入高炉,其目的是增大反应物的接触面积,使其充分反应。
(3)高炉气体的主要成分是氮气。炉渣主要成分是硅酸钙(CaSiO3),其中元素Ca、Si、O的质量比是40:28:(16×3)=10:7:12。
(4)从铁矿石得到单质铁,铁的化合价由+3降低到0。
(5)根据金属活动顺序,可以用锌与FeSO4溶液反应得到单质铁和硫酸锌,方程式是Zn+FeSO4=ZnSO4+Fe。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案【题目】实验探究题
(实验回顾)18世纪末,英国科学家普利斯特里和卡文迪许把“易燃空气”与空气或氧气混合后盛在干燥、洁净的玻璃瓶中,当用电火花点火时,发出震耳的爆鸣声,且玻璃瓶内壁上出现了液滴。一年之后,拉瓦锡重复了他们的实验,并做了一个相反的实验:让水蒸气通过一根烧红的枪管,得到了“易燃空气”。这里的“易燃空气”是指_____(填化学式)
(实验重现)某化学兴趣小组的同学在创新的基础上,在实验室中重做上述两个实验,做法如下:
实验1:水的通电分解实验
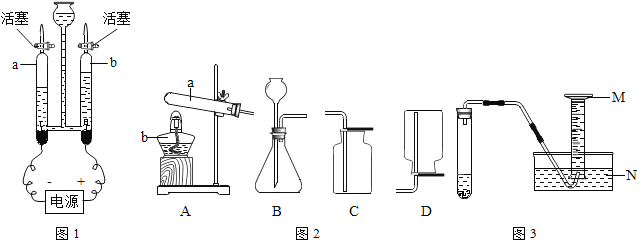
如图1所示,打开活塞b,用燃着的木条在玻璃管尖嘴口检验反应产生的气体,看到的现象是_____,证明该气体为_____。写出水的通电分解反应的化学方程式_____,
实验2:“易燃空气”与氧气混合后的点燃实验
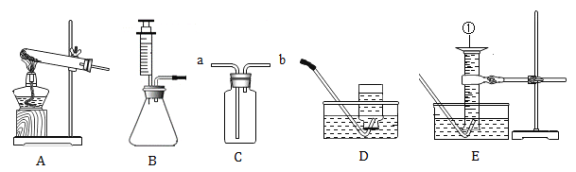
实验室现有过氧化氢溶液、高锰酸钾、二氧化锰、稀硫酸、锌粒,图2是实验室常用部分仪器:
(1)①仪器的名称:a是_____。
②实验室制取氧气的化学方程式为_____(写一个),实验时对应的气体发生和收集装置分别是_____(填标号,下同)和_____。
(2)实验室利用锌和稀硫酸制取较多量的“易燃空气”,且可以随时补充液体,你选择的装置是_____(填序号)。
(3)验纯后用装满水的10mL量筒代替小试管收集“易燃空气”,装置如图3所示。
①10mL量筒的最大刻度靠近_____端。(填写“M”或“N”)
②当10mL量筒中的水全部被排尽后,实际收集到的“易燃空气”体积V_____10.0mL.(填写“>”、“=”或“<”)
(4)该兴趣小组的同学决定利用制得的“易燃空气”和空气继续进行探究,他们取7支试管,依次盛水90%(体积分数)、80%…再用排水集气法收集“易燃空气”,而后分别把试管口移近酒精灯的火焰,实验结果如下表所示:
分析表中信息,完成下列问题:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
“易燃空气”体积分数(%) | 90 | 80 | 70 | 50 | 20 | 10 | 5 |
空气体积分数(%) | 10 | 20 | 30 | 50 | 80 | 90 | 95 |
点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱的爆鸣声 | 强的爆鸣声 | 强的爆鸣声 | 弱的爆鸣声 | 不燃烧 不爆鸣 |
①在混合气体爆炸范围内,“易燃空气”的体积分数约为_____;
②你对燃烧或燃烧条件的新认识是_____。