题目内容
【题目】已知20g氢氧化钠溶液与10g氯化镁溶液恰好完全反应,反应结束后过滤,滤液的质量为27.1g(不考虑实验过程的损失)。(反应的化学方程式:2NaOH + MgCl2 =Mg(OH)2↓ + 2NaCl )计算:
(1)反应生成的Mg(OH)2的质量为多少。
(2)参加反应的氢氧化钠溶液的溶质质量分数?(写出计算过程)
【答案】(1)2.9g (2)20%
【解析】
(1)根据质量守恒定律,反应前后的质量减少量即为氢氧化镁的质量,反应生成的Mg(OH)2的质量为20g+10g-27.1g=2.9g。
(2)解:设参加反应的NaOH 的质量为![]() ,
,
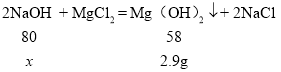
![]()
![]() = 4.0g
= 4.0g
则参加反应的氢氧化钠溶液的溶质质量分数为:![]()
答:参加反应的氢氧化钠溶液的溶质质量分数为20% 。

练习册系列答案
相关题目
【题目】甲、乙、丙三种物质的转化关系如图所示,“→”表示反应可以一步实现(部分物质和反应条件已省略),下面选项中不能按图示转化关系实现的是
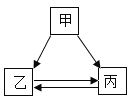
选项 | 甲 | 乙 | 丙 |
A | H2SO4 | H2O | H2 |
B | NaOH | NaCl | NaNO3 |
C | C | CO2 | CO |
D | Ca (OH) 2 | CaCl2 | CaCO3 |
A.AB.BC.CD.D