题目内容
【题目】
过氧化氢的分解的变化可用下式表示:
过氧化氢![]() 水+氧气
水+氧气
上述变化所涉及的物质中,属于金属氧化物的是 ,氧元素的化合价为—1价的是 。
用氯酸钾或过氧化氢制取氧气的实验中,都需要加入少量二氧化锰,二氧化锰的作用是 ;若未加入二氧化锰,则反应 (选填“不能发生”或“明显减慢”)
若实验室要制取48g氧气,至少需要氯酸钾多少克?
【答案】(1)二氧化锰(或MnO2)(1分) 过氧化氢(或H2O2)(1分)
(2)加快反应速率(或催化作用)(1分) 明显减慢(1分)
(3)解:设需要KClO3的质量为x。 (0.5分)
2KClO3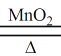 2KCl + 3O2↑ (1分)
2KCl + 3O2↑ (1分)
245 96 (2分)
x 48g
![]() =
=![]() (1分)
(1分)
x=122.5g (1分)
答:至少需要氯酸钾的质量为122.5g。
【解析】(1)金属氧化物是指由金属元素与氧元素形成的氧化物。二氧化锰中是锰、氧两种元素的化合物,属于金属氧化物。
根据化学式可计算出:在反应中的四种物质H2O2、MnO2、H2O、O2中,氧元素的化合价依次为-1、-2、-2、0。
(2)在加热氯酸钾和二氧化锰的混合物制氧气中,二氧化锰作催化剂,起催化作用;
在用过氧化氢和二氧化锰制取氧气的实验中,二氧化锰作催化剂,起催化作用。二氧化锰在两个实验中都起到了加快反应速率的作用。
催化剂的作用是改变化学反应的速率,本身的质量和化学性质在反应并未改变。所以在这两个反应中如不加入二氧化锰反应也可发生,只是速度要比加二氧化锰明显减慢。
(3)解题思路:已知氧气的质量为48g,求需要氯酸钾的质量。可根据用氯酸钾制氧气的反应中二者的质量关系进行计算。具体解题过程:
解:设需要KClO3的质量为x。 设未知量
2KClO3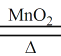 2KCl + 3O2↑ 写出反应的化学方程式
2KCl + 3O2↑ 写出反应的化学方程式
245 96 找出氯酸钾与氧气的质量比
x 48g 标出二者在反应中实际质量比
![]() =
=![]() 根据标出数值列比例式
根据标出数值列比例式
x=122.5g 求解未知量
答:至少需要氯酸钾的质量为122.5g。 写出答案

【题目】
[查阅资料]有些水果、蔬菜对过氧化氢的分解有催化作用。
[实验探究1]探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果:
各量取6ml的过氧化氢溶液,分别倒入1、2、3号三志试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管口内,观察现象并记录如下:
试管编号 | 1 | 2 | 3 | |
材料名称 | 无 | 苹果 | 土豆 | |
实验现象 | 反应速率 | 很慢 | 稍快 | 较快 |
产生气泡 | 很少 | 比1中多 | 较多 | |
复燃情况 | 不复燃 | 复燃 | 很快复燃 | |
实验结论 | ||||
[实验探究2]探究浓度对过氧化氢分解速率的影响:
取10ml30%的过氧化氢三份,将其中两份分别稀释为不同浓度的溶液,同时测定收集到100ml氧气所用的时间,(其它实验条件均相同)记录如下:
实验编号 | 1 | 2 | 3 |
过氧化氢溶液浓度 | 5% | 15% | 30% |
所用时间(秒) | 205 | 25 | 3 |
实验结论 | |||
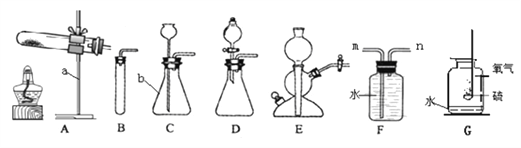
[实验条件3]用上述收集的仪器与不同位置进行反应,其中有一固体能在氧气中燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,该反应的化学方程式为: 。