题目内容
【题目】氧气和二氧化碳是两种重要的气体,请根据学过的知识作答:
①工业上用分离液态空气的方法制取氧气,主要是利用了氧气和氮气的________不同。二氧化碳的工业制法与实验室制法都选择了大理石,不仅因为这种原料含有________(填“钙元素”或“碳酸根”),而且来源非常广泛。
②根据所给的仪器回答问题
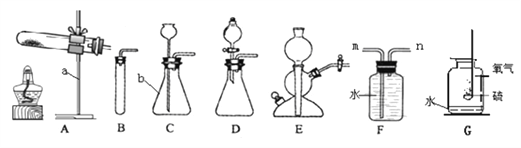
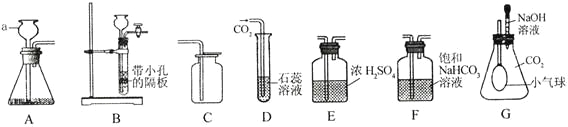
I.写出仪器名称,a ________、b _____________;
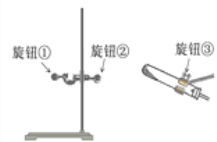
II.某同学用A装置制取氧气时发现试管位置太高,不能用外焰加热,该同学应调节下图中的旋钮_______(填“①”或“②”或 “③”)。
利用改正后的A装置制取氧气,反应的化学方程式:________________,若用装置F收集并粗略测出收集O2体积,还需在_________(填m或n)端接一个量筒以便测出排出的水的体积。G图是硫在氧气中燃烧的实验,观察到的现象是_____________,该反应的化学方程式是_________________________;
III.实验室也能选用D装置作为氧气发生装置,反应的化学方程式是________,为了使反应能保持较平稳地进行,应该采取的措施是___________ ;
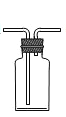
IV.B、C、D、E均可作为实验室制备CO2的发生装置,E装置制备气体的优点是__________,若用C装置制备CO2,操作时一定要___________,形成液封以免气体从长颈漏斗逸出;若用右图装置排空气法收集CO2,请在图中用箭头画出气体进出的方向_________。
V.用足量的石灰石和50克稀盐酸充分完全反应,制得二氧化碳为8.8克。试计算:
50克稀盐酸中所含HCl的物质的量(根据化学方程式列式计算);________________
稀盐酸中HCl的质量分数为___________ 。
【答案】 沸点 碳酸根 铁架台 锥形瓶 ② 2KClO3 ![]() 2KCl+3O2↑ m 产生蓝紫色火焰,有刺激性气味气体产生 S+O2点燃SO2 2H2O2=2 H2O+ O2↑ 控制分液漏斗的活塞,使液体缓缓流入锥形瓶 随开随用,随关随停 使长颈漏斗末端插入到液面下
2KCl+3O2↑ m 产生蓝紫色火焰,有刺激性气味气体产生 S+O2点燃SO2 2H2O2=2 H2O+ O2↑ 控制分液漏斗的活塞,使液体缓缓流入锥形瓶 随开随用,随关随停 使长颈漏斗末端插入到液面下 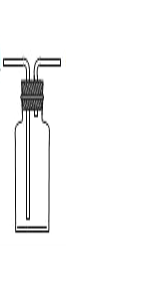 设所含HCl的物质的量xmol
设所含HCl的物质的量xmol
n(CO2)=8.8/44=0.2mol
CaCO3+2HCl = CaCl2+CO2↑+H2O
2 1 2/x=1/0.1
x 0.2 x=0.4mol 29.2%
【解析】根据所学知识和题中信息知,①工业上用分离液态空气的方法制取氧气,主要是利用了氧气和氮气的沸点不同。二氧化碳的工业制法与实验室制法都选择了大理石,不仅因为这种原料含有碳酸根,而且来源非常广泛。②根据所给的仪器回答问题。仪器名称,a铁架台、b锥形瓶;II.某同学用A装置制取氧气时发现试管位置太高,不能用外焰加热,该同学应调节右图中的旋钮②(填“①”或“②”或 “③”)。利用改正后的A装置制取氧气,反应的化学方程式:2KClO3![]() 2KCl+3O2↑。若用装置F收集并粗略测出收集O2体积,还需在m端接一个量筒以便测出排出的水的体积。G图是硫在氧气中燃烧的实验,观察到的现象是产生蓝紫色火焰,有刺激性气味气体产生. 该反应的化学方程式是S+O2
2KCl+3O2↑。若用装置F收集并粗略测出收集O2体积,还需在m端接一个量筒以便测出排出的水的体积。G图是硫在氧气中燃烧的实验,观察到的现象是产生蓝紫色火焰,有刺激性气味气体产生. 该反应的化学方程式是S+O2![]() SO2 .
SO2 .
III. 实验室也能选用D装置作为氧气发生装置,反应的化学方程式是2H2O2=2 H2O+ O2↑ ,为了使反应能保持较平稳地进行,应该采取的措施是控制分液漏斗的活塞,使液体缓缓流入锥形瓶;IV.B、C、D、E均可作为实验室制备CO2的发生装置,E装置制备气体的优点是. 随开随用,随关随停,若用C装置制备CO2,操作时一定要使长颈漏斗末端插入到液面下,形成液封以免气体从长颈漏斗逸出;若用右图装置排空气法收集CO2,请在图中用箭头画出气体进出的方向:右进左出。
V.用足量的石灰石和50克稀盐酸充分完全反应,制得二氧化碳为8.8克。试计算:
50克稀盐酸中所含HCl的物质的量(根据化学方程式列式计算);
解:设所含HCl的物质的量xmol
n(CO2)=8.8/44=0.2mol
CaCO3+2HCl= CaCl2+CO2↑+H2O
2 1
x 0.2
2/x=1/0.1 x=0.4mol
稀盐酸中HCl的质量分数为﹙0.4mol×36.5g/mol﹚/50g×100%=29.2%
答; 所含HCl的物质的量是0.4mol,稀盐酸中HCl的质量分数为29.2%。