题目内容
【题目】请根据题目要求回答下列问题。
(1)在小烧杯中加入硫酸铜溶液后,加入铁钉,称量总质量为m1,发生反应的化学方程式为_____,反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为 m2,(假设水不蒸发),则(填“=”“>”“<”)m1_____ m2。
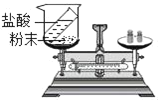
(2)如图装置中,称量小烧杯中所有物质的质量m1,然后将小烧杯中的铝粉与盐酸完全混合,发生反应的化学方程式为_____,反应发生了一段时间后,再称量小烧杯及烧瓶内物质的总质量为 m2,(假设水和氯化氢不蒸发),则(填“=”“>”“<”)m1_____m2,该反应_____(填“遵循”或“不遵循”)质量守恒定律。
(3)关于化学变化前后相关的说法正确的是_____
A 分子种类一定不变 B 原子种类一定不变
C 化学变化不一定都遵循质量守恒 D 元素种类一定不变
【答案】Fe+CuSO4=Cu+FeSO4 = 2Al+6HCl=2AlCl3+3H2↑ > 遵循 BD
【解析】
硫酸铜和铁反应生成硫酸亚铁和铜,铝和盐酸反应生成氯化铝和氢气。根据质量守恒定律,化学反应前后,元素种类不变,原子个数、种类、质量不变
(1)硫酸铜和铁反应生成硫酸亚铁和铜,化学方程式为:![]() ,反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为 m2,则m1=m2。
,反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为 m2,则m1=m2。
(2)铝和盐酸反应生成氯化铝和氢气,化学方程式为:![]() ,反应发生了一段时间后,再称量小烧杯及烧瓶内物质的总质量为 m2,氢气逸散到空气中,则m1>m2,该反应遵循质量守恒定律。
,反应发生了一段时间后,再称量小烧杯及烧瓶内物质的总质量为 m2,氢气逸散到空气中,则m1>m2,该反应遵循质量守恒定律。
(3)根据质量守恒定律,化学反应前后,元素种类不变,原子个数、种类、质量不变,故选:BD。

练习册系列答案
相关题目