题目内容
【题目】氯化钠是日常生活中的必需品,某氯化钠样品中除含氯化钠外,还含有少量的CaCl2和MgCl2以及不溶性杂质,以下是提纯该样品的操作流程图
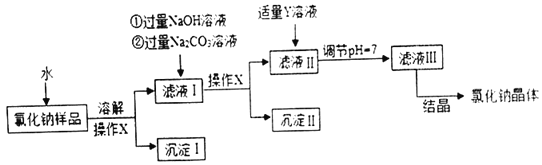
下列说法不正确的是( )
A. 操作X的名称是过滤
B. Y溶液中溶质的化学式是HCl
C. 上述操作流程中共发生3个复分解反应
D. 该流程发生的化学反应中,NaOH+HCl=NaCl+H2O属于中和反应
【答案】C
【解析】
A、作X的名称是过滤,通过过滤除去不溶于水的物质,该选项说法正确;
B、Y溶液是稀盐酸,稀盐酸中的溶质的化学式是HCl,该选项说法正确;
C、上述操作流程中共发生4个复分解反应,即氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳,该选项说法不正确;
D、稀盐酸和氢氧化钠反应生成氯化钠和水,是酸碱中和反应,该选项说法正确。
故选:C。

【题目】实验室中有一瓶标签受损的无色溶液,如图1所示,老师提示这是一瓶初中常用的溶液,要求同学们确认其溶质成分。
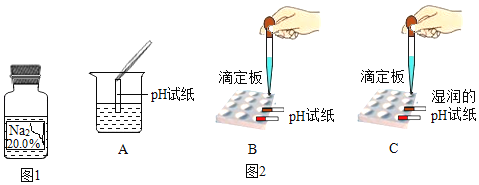
【提出猜想】①氯化钠②氢氧化钠③硫酸钠④碳酸钠
【查阅资料】氯化钠和硫酸钠溶液pH=7可溶性硫酸盐遇到可溶性的钡盐会产生白色沉淀。
【讨论分析】经过讨论,同学们一致认为猜想_____(填序号)不成立,其原因是_____。
【实验探究】为了进一步确认其成分,同学们继续进行探究:
实验步骤 | 实验现象 | 实验结论 |
(1)取该溶液少许于试管中,向其中滴加稀盐酸 | 无明显现象 | 猜想_____不成立 |
(2)取该溶液少许于试管中,向其中滴加氯化钡溶液 | _____________ | 猜想③成立 |
假如猜想④成立,写出(1)中发生的反应方程式_____。
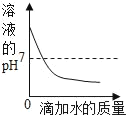
【反思与交流】有同学提出用测pH的方法也可以确定该无色溶液,如图2所示是几位同学的实验过程,其中正确的是_____。
【题目】某化学小组同学对NaOH的化学性质进行如下实验探究。
实验一:NaOH溶液与CO2的反应,装置及实验测定结果如下
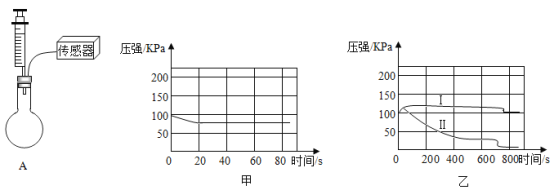
(1)某同学检验A装置气密性(夹持仪器省略),甲图象说明装置气密性良好,该同学进行的操作是_____。
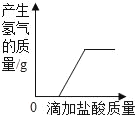
(2)在烧瓶中充满CO2图乙是用注射器向瓶中分别注入同体积水和NaOH溶液得到的压强变化图象,其中表示CO2与NaOH溶液发生反应的是_____(填“Ⅰ”或“Ⅱ”),该反应的化学方程式为_____。
实验二:NaOH溶液与Fe2(SO4)3溶液的反应
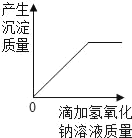
(3)实验操作如图B所示,反应的化学方程式为_____。

(4)充分反应后得到的无色溶液中一定含有的离子是_____(填离子符号)。
实验三:NaOH溶液与盐酸的反应
室温下,取10份相同体积溶质质量分数为10%的NaOH溶液于10个烧杯中,分别滴加一定体积溶质质量分数为10%的盐酸,并测定溶液温度,记录数据如下:
加入盐酸体积/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
测得溶液温度 | 25.2 | 28.6 | 32.0 | 36.0 | 38.2 | 36.7 | 35.7 | 34.7 | 33.7 | 32.9 |
(5)加入盐酸体积在12﹣20mL之间时,溶液温度下降的原因可能是①_____②_____。
(6)根据碱与酸反应的性质,可将Al(OH)3制成抗胃酸(主要成分为HCl)药剂,请回答:
①Al(OH)3的相对分子质量_____。
p>②0.25g Al(OH)3能消耗胃酸中的HCl_____g(结果精确到0.01)