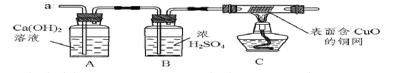题目内容
铁是重要的金属材料,在生产、生活中有广泛的用途。

探究一 比较生铁、纯铁与稀盐酸反应的速率
各取1g生铁和纯铁与足量的相同质量分数的稀盐酸反应,生成H2的量如图1所示(A、B分别表示纯铁、生铁和盐酸反应产生的氢气质量)。
(1)铁与盐酸反应的化学方程式是 (填序号).。
A.Fe+2HCl=FeCl2+H2↑ B.2Fe+6HCl=2FeCl3+3H2↑ C.Fe+HCl=FeHCl
(2)从图1可知:生铁与稀盐酸反应的速率 (填“大于”“小于”或“等于”)纯铁与稀盐酸反应的速率。
(3)图1中呈现出生铁生成的H2量少,其原因是: 。
探究二 温度对铁与盐酸反应速率的影响
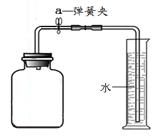
请你设计一个简单的实验探究案 。
探究三 测定生铁中的含碳量
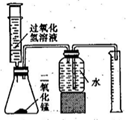
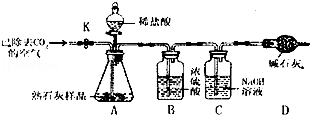
生铁中除铁外,还含有碳元素和硫元素。某兴趣小组设计图2所示的实验装置,测定生铁中的含碳量。【查阅资料】资料1:SO2和CO2气体都能与澄清的石灰水反应生成沉淀。资料2:SO2能和30%双氧水反应被吸收,CO2气体不与双氧水发生作用。
(4)实验过程中,该兴趣小组应注意的安全问题是 (任写一种)。
(5)待C管的样品充分反应后,测得E中生成的沉淀为2g,请计算出生铁中的含碳量为 %。
(6)若无D装置,所测定的含碳量将 (填“偏高”、“偏低”或“不影响”)。

探究一 比较生铁、纯铁与稀盐酸反应的速率
各取1g生铁和纯铁与足量的相同质量分数的稀盐酸反应,生成H2的量如图1所示(A、B分别表示纯铁、生铁和盐酸反应产生的氢气质量)。
(1)铁与盐酸反应的化学方程式是 (填序号).。
A.Fe+2HCl=FeCl2+H2↑ B.2Fe+6HCl=2FeCl3+3H2↑ C.Fe+HCl=FeHCl
(2)从图1可知:生铁与稀盐酸反应的速率 (填“大于”“小于”或“等于”)纯铁与稀盐酸反应的速率。
(3)图1中呈现出生铁生成的H2量少,其原因是: 。
探究二 温度对铁与盐酸反应速率的影响
请你设计一个简单的实验探究案 。
探究三 测定生铁中的含碳量
生铁中除铁外,还含有碳元素和硫元素。某兴趣小组设计图2所示的实验装置,测定生铁中的含碳量。【查阅资料】资料1:SO2和CO2气体都能与澄清的石灰水反应生成沉淀。资料2:SO2能和30%双氧水反应被吸收,CO2气体不与双氧水发生作用。
(4)实验过程中,该兴趣小组应注意的安全问题是 (任写一种)。
(5)待C管的样品充分反应后,测得E中生成的沉淀为2g,请计算出生铁中的含碳量为 %。
(6)若无D装置,所测定的含碳量将 (填“偏高”、“偏低”或“不影响”)。
(1)A;(2)大于;(3)生铁中主要的杂质是碳,碳与酸不反应,所以生铁与酸反应产生的氢气小于纯铁与酸反应生成的氢气质量;分别取相同质量的铁放入两支试管,向两支试管中加入足量相同的盐酸,一支试管加热,记录两支试管反应完需要的时间;(4)浓硫酸腐蚀性很强,在使用时注意安全,不要溅到身上(或用酒精喷灯加热时需要进行预热,防止炸裂导管,造成危险);(5)2.4;(6)偏高
试题分析:(1)铁与盐酸反应生成氯化亚铁和氢气,所以A答案正确;
(2)谁先到达最高点谁反应的速度快,由图可知生铁与稀盐酸反应的速率大于纯铁与稀盐酸反应的速率;
(3)生铁中主要的杂质是碳,碳与酸不反应,所以生铁与酸反应产生的氢气小于纯铁与酸反应生成的氢气质量;设计对照实验,变量是温度,其它条件必须相同,所以分别取相同质量的铁放入两支试管,向两支试管中加入足量相同的盐酸,一支试管加热,记录两支试管反应完需要的时间;
(4)该实验用到浓硫酸腐蚀性很强,在使用时注意安全,不要溅到身上;用酒精喷灯加热时需要进行预热,防止炸裂导管,造成危险;
(5)设生成2g碳酸钙沉淀需要参加反应的二氧化碳质量为X则:
CO2+Ca(OH)2=CaCO3↓+H2O
44 100
x 2g
根据
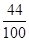 =
=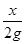 解得:X=0.88g
解得:X=0.88g二氧化碳中碳元素质量为:0.88g×
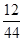 ×100%=0.24g
×100%=0.24g生铁中的含碳量为:
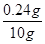 ×100%=2.4%;
×100%=2.4%;(6)无D装置二氧化硫也能与氢氧化钙反应生成沉淀,把它误认为是二氧化碳,算出的二氧化碳质量偏大,计算出的碳质量偏大,所以碳的质量分数偏高。

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目