题目内容
【题目】我国制碱工业先驱侯德榜发明了“侯氏制碱法”.其模拟流程如图所示: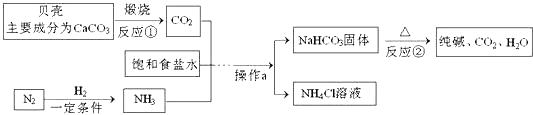
(1)反应①的化学方程式 , 反应②的基本反应类型为。
(2)工业上用分离液态空气的方法制取氮气,属于变化(填“物理”或“化学”)。
(3)操作a的名称是 , 实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、。
(4)从物质的类别看,NH4Cl属于(选填“酸”“碱”或“盐”)。
【答案】
(1)CaCO3 ![]() CaO+CO2↑,分解
CaO+CO2↑,分解
(2)物理
(3)过滤,漏斗
(4)盐
【解析】根据所学知识和题中信息可知:
(1)反应①的化学方程式是CaCO3 ![]() CaO+CO2↑,反应②的基本反应类型为分解反应;
CaO+CO2↑,反应②的基本反应类型为分解反应;
(2)工业上用分离液态空气的方法制取氮气,属于物理变化;
﹙3)操作a的名称是过滤;实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(4)从物质的类别看,NH4Cl属于盐.
所以答案是:(1)CaCO3 ![]() CaO+CO2↑,分解;
CaO+CO2↑,分解;
(2)物理;
﹙3)过滤;漏斗;
(4)盐.

【题目】某化学兴趣小组的同学在做氢氧化钙与稀盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应。于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告。
Ⅰ.定性探究
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性。
(1)【猜想与假设】
猜想Ⅰ:溶液中的溶质只有
猜想Ⅱ:溶液中的溶质有CaCl2、HCl
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl
(2)请写出该反应的化学方程式。经过讨论,同学们直接得出不合理的猜想是哪一种并说出理由。为了验证余下的哪一种猜想是正确的,同学们又做了以下实验。
(3)【进行实验】
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞溶液 | 猜想Ⅲ不正确 | |
②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钠 | 有气泡产生 | 猜想不正确 |
(4)操作②有气泡生成的化学方程式为。
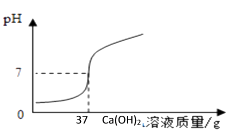
(5)下列曲线能够表示所做实验中溶液pH变化趋势的是 (填序号)。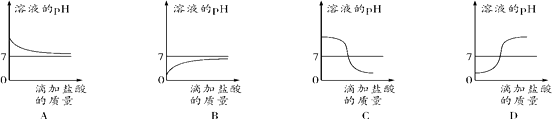
(6)【反思交流】
要使烧杯内溶液的溶质只含CaCl2 , 需要除去杂质,其中的一种方法是向烧杯中加入过量的 , 然后过滤。
(7)II.定量探究
兴趣小组同学想对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钙溶液进行中和,如下图所示.请你计算废水中盐酸的溶质质量分数(写出具体的计算过程)