题目内容
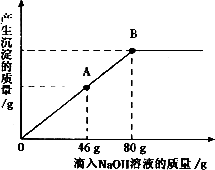
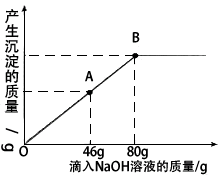
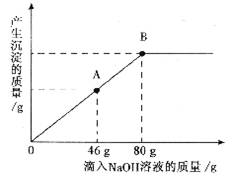
 在一烧杯中盛有一定质量的CaCO3固体,向其中滴加溶质质量分数为7.3%的稀盐酸至恰好完全反应,得到120g不饱和溶液,再向其所得溶液中加入溶质质量分数为10%的Na2CO3溶液,产生沉淀的质量与所滴入Na2CO3溶液的质量关系如图所示.请根据题意回答下列问题:
在一烧杯中盛有一定质量的CaCO3固体,向其中滴加溶质质量分数为7.3%的稀盐酸至恰好完全反应,得到120g不饱和溶液,再向其所得溶液中加入溶质质量分数为10%的Na2CO3溶液,产生沉淀的质量与所滴入Na2CO3溶液的质量关系如图所示.请根据题意回答下列问题:(1)在滴入稀盐酸时,观察到的1项明显现象
有气泡出现
有气泡出现
.(2)当滴入Na2CO3溶液至图中A点时,烧杯里溶液中含有的溶质是(填化学式)
CaCl2
CaCl2
、NaCl
NaCl
.(3)当滴入10%的碳酸钠溶液106g(即B点)时,试通过计算,求此时烧杯中所得不饱和溶液的质量.
分析:(1)依据盐酸与碳酸钙反应时会生成二氧化碳的有关结论分析反应的现象;
(2)依据A点是碳酸钠量不足而氯化钙有剩余的知识分析解答;
(3)利用方程式求出生成的碳酸钙质量,而后利用质量守恒定律即可求出溶液的质量;
(2)依据A点是碳酸钠量不足而氯化钙有剩余的知识分析解答;
(3)利用方程式求出生成的碳酸钙质量,而后利用质量守恒定律即可求出溶液的质量;
解答:解:(1)由于盐酸与碳酸钙反应时会生成二氧化碳,所以会观察到有气泡出现的明显现象;
(2)当滴入Na2CO3溶液至图中A点时,两者没有完全反应氯化钙有剩余,所以烧杯中的溶液中含有反应生成NaCl和剩余的CaCl2;
(3)设生成碳酸钙的质量是x
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100
106g×10% x
=
x=10g
所以所得溶液的质量是120g+106g-10g=216g
故答案为:(1)有气泡出现;(2)CaCl2;NaCl;(3)此时烧杯中所得不饱和溶液的质量为216g;
(2)当滴入Na2CO3溶液至图中A点时,两者没有完全反应氯化钙有剩余,所以烧杯中的溶液中含有反应生成NaCl和剩余的CaCl2;
(3)设生成碳酸钙的质量是x
CaCl2+Na2CO3=CaCO3↓+2NaCl
106 100
106g×10% x
| 106 |
| 106g×10% |
| 100 |
| x |
x=10g
所以所得溶液的质量是120g+106g-10g=216g
故答案为:(1)有气泡出现;(2)CaCl2;NaCl;(3)此时烧杯中所得不饱和溶液的质量为216g;
点评:本题属于数形结合型计算,由表示反应过程的曲线获得恰好完全反应即曲线的折点时的相关数据时,体现对问题的分析能力.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目