题目内容
【题目】图甲是A、B、C三种固体物质的溶解度曲线图。

①甲图中,t2℃时,A、B、C三种物质中溶解度最大的是____________。P点表示____________。
②将t2℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,三种物质的溶液中溶质质量分数由大到小的顺序是_____________________。
③如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小块生石灰,再加入5mL水,几分钟后烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的______________(填写物质编号),试管内发生的化学反应方程式为________________。
④t2℃时,B物质的溶解度为40g/100g水,在150g水中投入_____________g的B物质,溶液将达到饱和。
【答案】①A;t1℃时,B、C两种物质的溶解度相等;
②B>C>A;
③C;CaO+H2O![]() Ca(OH)2;
Ca(OH)2;
④60
【解析】
试题分析:①从甲图可知,t2℃时,A、B、C三种物质中溶解度最大的是A;P点为在t1℃时,B和C的溶解度曲线的交点,说明此时两物质的溶解度相等;
②将t2℃时的A、B、C三种物质的饱和溶液,降温至t1℃时,由于A、B物质的溶解度随温度的降低而减小,所以都有晶体析出,此时溶解度B>A,而C物质溶解度随温度的降低而升高,所以溶液变 为不饱和溶液,质量分数不变,此时A物质的溶解度小于开始时C物质的溶解度,B物质的溶解度大于开始时C物质的溶解度,根据饱和溶液的溶解度越大,对应溶液溶质的质量分数越大的规律可知,A、B、C三种物质的溶液中溶质的质量分数由大到小的顺序是B>C>A;
③由于生石灰和水的反应是放热反应,烧杯内的溶液出现浑浊,说明该物质的溶解度随着温度的升高而减小,则X可能为A、B、C三种固体物质中的C;氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O![]() Ca(OH)2;
Ca(OH)2;
④设150g水中投的B物质的质量为m;则m:150g=40g:100g;得:m=60g;即t2℃时,B物质的溶解度为40g/100g水,在150g水中投入60g的B物质,溶液将达到饱和。

 导学全程练创优训练系列答案
导学全程练创优训练系列答案【题目】某兴趣小组按下图所示装置制取二氧化碳,并检验二氧化碳的性质:
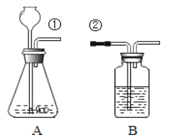
(1)若用装置B来证明二氧化碳能与水反应生成碳酸,B中除有少量水外,还应加入的试剂是 ,当①、②导管口连接时,B中看到的实验现象是 ,反应的化学方程式是 。
(2)他们从我市一古建筑维修现场搜集了一些旧墙灰,通过查阅资料得知:古建筑旧墙灰的主要成分是碳酸钙。他们称取了12.0g旧墙灰放入烧杯中,并加入足量稀盐酸(假设杂质不参与反应,不考虑H2O、HCl的逸出)。反应开始时,烧杯及所盛物质的总质量为300.0g。实验数据记录如下:
反应时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
烧杯及所盛物质的总质量/g | 300.0 | 299.0 | 298.0 | 297.2 | 296.5 | 296.0 | 295.7 | 295.6 | M | 295.6 |
①以该小组因故没有记录反应时间为16min时的数据M,由表中数据推测,M=_______g
②反应生成二氧化碳的总质量为__________________(列出算式)。
③旧墙灰中碳酸钙的质量分数(写出计算过程)。