题目内容
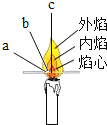
【题目】物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成一次有效进攻。场上“队员”位置及传球路线如图所示。
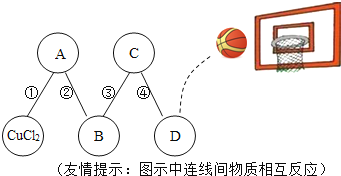
(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是________;
(2)B位置“队员”所代表物质的一种用途是________;
(3)写出连线④代表的物质间发生反应的化学方程式________;连线①代表的物质间发生化学反应的基本类型是________反应。
【答案】CO2(或二氧化碳) 金属除锈(或生产化肥、农药、火药、燃料等) Ca(OH)2+ CO2= CaCO3↓+H2O 置换
【解析】
首先根据“D位置上投篮的‘队员’是个灭火‘能手’”可知D为二氧化碳,根据C、D间能反应,在五种物质中能与二氧化碳反应的物质是氢氧化钙,即C是氢氧化钙,剩余二种物质中能与氢氧化钙反应的物质是硫酸,所以B是硫酸,最后剩下A为铁。
(1)由分析可知,D 是CO2(或二氧化碳);
(2) B是硫酸,可用于金属除锈(或生产化肥、农药、火药、燃料等);
(3)连线④表示氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+ CO2= CaCO3↓+H2O;连线①表示氯化铜和铁反应生成氯化亚铁和铜,该反应是一种单质与一种化合物反应生成另一种单质与另一种化合物的反应,属于置换反应。

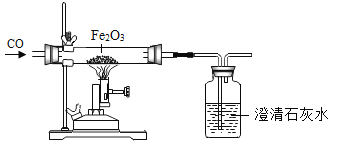
【题目】实验室常用二氧化锰催化过氧化氢溶液分解的方法制取氧气。该实验速率快,产物无污染,某实验小组进行了如下探究。
(探究实验)书本介绍了除了用二氧化锰外,硫酸铜溶液也可以催化过氧化氢溶液的分解,查阅资料得知,氯化铁溶液也可以催化过氧化氢溶液的分解。那么,硫酸铜溶液和氯化铁溶液催化的效果怎么样呢?请根据下表四组实验现象,回答下面问题
序号 | 催化剂 | 实验步骤 | 实验现象 | 实验结论 |
1 | FeC13溶液 | 向5mL4%的H2O2溶液,滴5滴0.1%FeC13溶液 | 试管中产生大量气泡 | FeC13溶液对H2O2的分解有较好的催化效果 |
2 | FeC13溶液 | 向5mL12%的H2O2溶液,滴5滴0.1%FeC13溶液 | 试管中有适量气泡 | |
3 | CuSO4溶液 | 向5mL4%的H2O2溶液,滴5滴0.1%CuSO4溶液 | 试管中产生少量气泡 | CuSO4溶液对H2O2的分解催化效果一般 |
4 | CuSO4溶液 | 向5mL12%的H2O2溶液,滴5滴0.1%CuSO4溶液 | 试管中气泡量很少 |
(思考分析)
(1)CuSO4属于______(填“酸”或“碱”或“盐”)
(2)请你写出用二氧化锰催化过氧化氢溶液分解的反应方程式______。
(3)通过实验____(填序号)可以比较硫酸铜溶液和氯化铁溶液催化过氧化氢溶液分解的效果。
(4)请你从上面的实验,选择一组合适的药品进行实验室制取氧气,____%H2O2溶液,______(填催化剂的种类和浓度)。
(5)从上面的实验中,你还能得到什么结论______。
(拓展延伸)
(6)在老师的鼓励下,同学们继续探究FeCl3溶液中到底是哪种粒子催化H2O2的分解,请你设计一组实验进行探究______。
(7)另一名同学了解到,加热也可促进过氧化氢溶液分解,于是进行如下实验,分别取5mL12%的H2O2溶液于试管中进行水浴加热,步骤和现象如下:
序号 | 加热耗时 | 水浴温度 | 分解现象 |
1 | 12分 | 65℃ | 少量气泡 |
2 | 15分 | 74℃ | 明显气泡 |
3 | 21分 | 87℃ | 大量气泡 |
根据该同学的探究,试分析回答,为什么实验室通常不用加热过氧化氢溶液的方法制氧气?(两点理由):______。
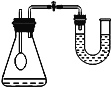
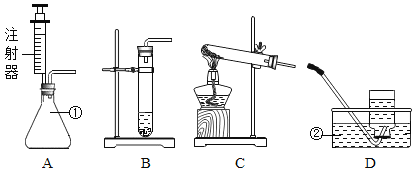
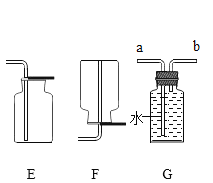
【题目】分类法在日常生活和科学研究中具有广泛的应用。化学实验可以按照实验目的分为:“探究物质性质实验、探究物质含量实验、探究反应条件实验”等。请回答问题:
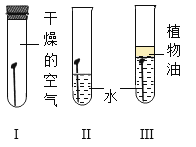
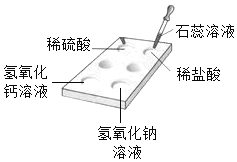
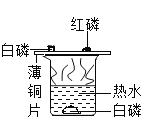
(1)我们可以将实验D与实验_____(填字母)分为一类,分类依据是________。
A | B | C | D |
|
|
|
|
(2)某同学做中和反应实验时,用pH传感器测得溶液的pH变化如图所示。
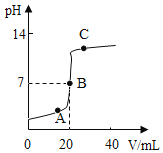
①向A点溶液中滴加紫色石蕊溶液,实验现象是______
②C点溶液中有_____种溶质。