题目内容
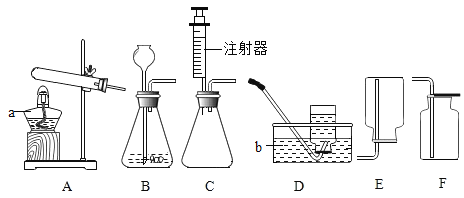
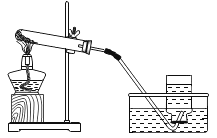
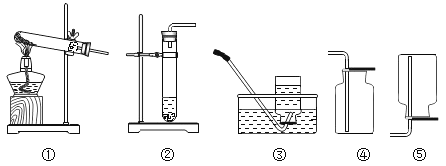
【题目】如图是实验室制取气体的一些装置,据图回答有关问题。
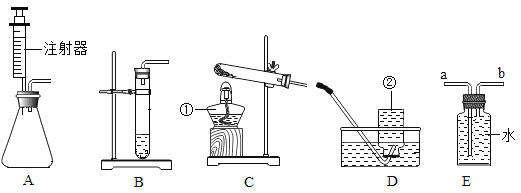
(1)写出指定仪器的名称:①_____;②_____;
(2)写出一个实验室用装置B制取气体的文字表达式_____
(3)加热高锰酸钾制取氧气,其发生装置为_____(填编号,下同),收集较纯净的氧气最好用_____装置。则当实验中观察到_____现象时可以开始收集气体。反应的文字表达式为:_____,此反应属于_____反应。
(4)加热高锰酸钾制氧气放团棉花的原因是_____。实验结束后要先将导管移出水面后熄灭酒精灯,原因是_____。
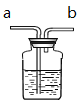
(5)实验室在常温下用块状电石与水反应制取乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。你认为上图中最适合制取乙炔气体的发生装置是_____(填装置序号);如果用E图所示装置收集乙炔,气体应从_____(填“a”或“b”)端管口通入。
【答案】试管 集气瓶 过氧化氢![]() 水+氧气 C D 气泡连续均匀冒出 高锰酸钾
水+氧气 C D 气泡连续均匀冒出 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 分解 防止高锰酸钾粉末进入导管 防止水槽中的水倒流,炸裂试管 A b
锰酸钾+二氧化锰+氧气 分解 防止高锰酸钾粉末进入导管 防止水槽中的水倒流,炸裂试管 A b
【解析】
(1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气进行分析;
(3)根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,排水法收集的氧气纯净,当实验中观察到气泡连续均匀冒出现象时可以开始收集气体,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(4)根据加热高锰酸钾制氧气放团棉花的原因是:防止高锰酸钾粉末进入导管,实验结束后要先将导管移出水面后熄灭酒精灯,原因是:防止水槽中的水倒流,炸裂试管进行分析;
(5)根据实验室制取乙炔的反应物是固体和液体,反应条件是常温,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂,乙炔不易溶于水进行分析。
(1)通过分析题中所指仪器的名称和作用可知,①是试管,②是集气瓶;
(2)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,文字表达式为:过氧化氢![]() 水+氧气;
水+氧气;
(3)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以发生装置为C,排水法收集的氧气纯净,所以收集较纯净的氧气最好用D装置,当实验中观察到气泡连续均匀冒出现象时可以开始收集气体,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气,该反应属于分解反应;
锰酸钾+二氧化锰+氧气,该反应属于分解反应;
(4)加热高锰酸钾制氧气放团棉花的原因是:防止高锰酸钾粉末进入导管,实验结束后要先将导管移出水面后熄灭酒精灯,原因是:防止水槽中的水倒流,炸裂试管;
(5)实验室制取乙炔的反应物是固体和液体,反应条件是常温,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂,乙炔不易溶于水,所以上图中最适合制取乙炔气体的发生装置是A,如果用E图所示装置收集乙炔,气体应从b端管口通入。

【题目】酒精灯是实验室中常用加热仪器,某兴趣小组同学对酒精灯进行如下探究。
(Ⅰ)定性研究甲同学取一根火柴梗,拿住一端迅速平放入酒精灯火焰中,1~2s后取出,观察到位于焰心的部分没有明显变化,说明焰心温度最低。
(1)写出碳完全燃烧的文字表达式(或符号表达式)__________。
(Ⅱ)定量研究
乙同学用注射器抽取灯芯和焰心交界处气体,利用氧气传感器测量氧气的体积分数(见下表),丙同学利用高温传感器测定酒精灯灯芯和焰心交界处温度(见下表)。
测量次数 | 第一次 | 第二次 | 第三次 |
灯芯和焰心交界处 氧气体积分数 | 5.93% | 5.29% | 6.53% |
灯芯和焰心交界处温度/℃ | 236 | 243 | 240 |
(2)乙、丙同学多次进行测量的目的是_____。
(3)火柴梗燃烧需要氧气的最低含量是14.0%,着火点是270℃,结合上表谈谈你对“火柴梗在焰心处没有明显变化”的认识_____。
(4)如果考虑抽气时空气的影响,则乙同学测出的氧气浓度比焰心的实际氧气浓度_____。(填“高”或“低”):另外乙同学所测氧气的体积分数差异的原因可能是①_____;②_____。
【题目】课堂上,老师取20g蔗糖放入小烧杯中,加少量水使它润湿,注入10mL浓硫酸,搅拌,同学们看到蔗糖先变黑后“发酵”形成“黑面包”,同时还闻到了刺激性气味,同学们判断黑色固体是碳,原因是浓硫酸具有脱水性。
形成“黑面包”的主要原因是什么?在老师的指导下,同学们开展了探究活动.
(猜想与假设)浓硫酸与碳反应,生成大量气体使黑色固体膨胀.
(查阅资料)
Ⅰ.浓硫酸与碳在加热条件下反应,生成物中有SO2、CO2两种气体.
Ⅱ.SO2是一种具有刺激性气味的气体,能与Ca(OH)2溶液反应生成白色沉淀,也能与高锰酸钾溶液反应。
Ⅲ.SO2能使品红溶液褪色,而CO2不能.
(实验探究)
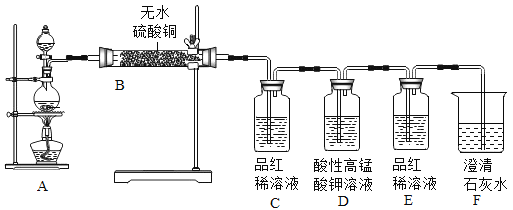
为验证碳与浓硫酸在加热条件下生成的气体产物,同学们在老师指导下设计并进行如图实验:
(事实与结论)
(1)请将能得出对应结论的实验现象填入表中.
验证气体 | 实验现象 | 实验结论 |
SO2 | _________ | 有SO2产生 |
CO2 | _________ | 有CO2产生 |
(2)碳与浓硫酸反应的化学方程式是:___________。
(3)浓硫酸与碳在加热条件下产生大量的SO2和CO2,使黑色固体膨胀,形成“黑面包”,猜想成立.
(反思与交流)
(1)小明同学提出,因老师的演示实验没有进行加热,所以同学们的探究实验无意义,其他同学一致否定了他的说法,理由是:_____________。
(2)在实验中看到B中无水硫酸铜变蓝,请写出B中反应的化学方程式:________。
(3)D中酸性高锰酸钾溶液的作用是:________, E中品红溶液的作用是:______。