��Ŀ����
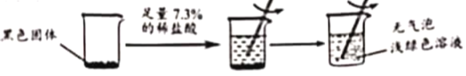
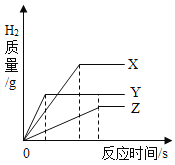
����Ŀ������ͬ�������ͬ��������������ϡ���ᣬ�ֱ���뵽��������������С��ͬ��X��Y��Z���ֽϻ��ý����У�������ȫ��Ӧ�����������о���+2�ۣ������������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ� ��
A.��������������˳��ΪX ��Y�� Z
B.���ֽ����Ļ��˳��ΪY��X��Z
C.�������������˳��ΪZ��Y��X
D.���ԭ�������ɴ�С��˳��ΪX��Y��Z
���𰸡�B
��������
A����ͼ���п��Կ�����Y��Ӧ����ʱ����̣��䷴Ӧ������죬Z����ʱ�������Ӧ��������A����
B����ͼ���п��Կ�����Y��Ӧ����ʱ����̣��䷴Ӧ������죬��������ǿ��Z����ʱ�������Ӧ��������Z�Ļ����������B��ȷ��
C�����ݷ�Ӧ��ԭ������֪���������е���Ԫ��ȫ��ת��Ϊ��������ͼ���п��Կ����������������Ӷൽ�ٵ�˳��Ϊ��X��Y��Z������������������ɶൽ�ٵ�˳��Ϊ��X��Y��Z����C����
D���ڻ��ϼ���ͬ�������£��������Ľ������������ᷴӦ�����ԭ������Խ�����������������Խ�٣���ͼ���п��Կ����������������Ӷൽ�ٵ�˳��Ϊ��X��Y��Z�������ԭ�������Ĵ�СΪ��X��Y��Z����D����
��ѡB��