题目内容
【题目】氮化镓可用作制芯片材料。如图是氮元素在元素周期表中的信息以及镓原子的结构示意图。下列说法不正确的是
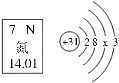
A.氮原子核内质子数为7
B.氮的相对原子质量为14.01
C.图中x=18
D.镓原子核内中子数为31
【答案】D
【解析】
A、元素周期表中的一格可以获得的信息:左上角的数字表示原子序数;原子序数=质子数,由图可知氮原子的核内质子数为7,正确;
B、元素周期表中的一格可以获得的信息:汉字下面的数字表示相对原子质量;由图可知氮的相对原子质量为14.01,正确;
C、镓元素的核内质子数为31,则其核外电子数也为31,故x=31-2-8-3=18,正确;
D、根据原子结构示意图可知,圆圈内有数字表示质子数,不表示中子数,根据原子结构图不能知道镓原子中的中子数为31,错误。
故选D。

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
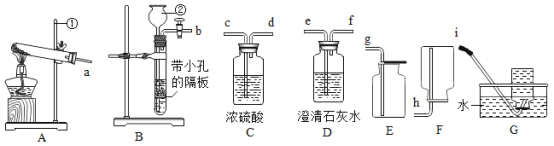
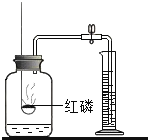
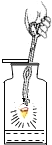
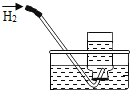
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是![]()
![]()
A | B | C | D | |
实 验 装 置 |
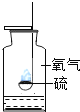
硫在氧气中燃烧 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
排水法收集氢气 |
解释 | 集气瓶中的水: 吸收有害气体 | 量筒中的水: 通过水体积的变化得出 | 集气瓶中的水: 吸收溅落融熔物 | 集气瓶中的水: 水先将集气瓶内的空气排净,后便于观察 |
A. A B. B C. C D. D