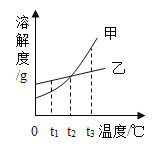
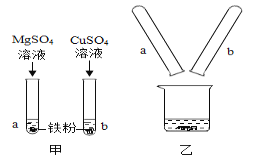
ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΡ≥Έό…Ϊ»ή“ΚΩ…ΡήΚ§”–CuSO4ΓΔCaCO3ΓΔNa2CO3ΓΔNa2SO4ΓΔMgCl2ΓΔNaCl÷–ΒΡ“Μ÷÷ΜρΕύ÷÷Θ§ΈΣΝΥ»ΖΕ®ΗΟ»ή“ΚΒΡ≥…Ζ÷Θ§Ϋχ––»γœ¬ Β―ιΘΚ
≤Ϋ÷ηΔώΘΚ»Γ…ΌΝΩ‘≠Έό…Ϊ»ή“Κ”Ύ ‘Ιή÷–Θ§Φ”»κΙΐΝΩΒΡBa(OH)2»ή“ΚΘ§…ζ≥…ΑΉ…Ϊ≥ΝΒμΘ§Ιΐ¬ΥΘ§ΒΟΒΫ¬Υ‘ϋAΚΆ¬Υ“ΚBΘ§œρ¬Υ‘ϋA÷–Φ”»κΙΐΝΩœΓœθΥαΥαΘ§ΑΉ…Ϊ≥ΝΒμ≤ΩΖ÷»ήΫβΘ§ΈόΤχ≈ί≤ζ…ζΓΘ
≤Ϋ÷ηΔρΘΚ»Γ≤Ϋ÷ηΔώ÷–ΒΡ¬Υ“ΚB”Ύ ‘Ιή÷–Θ§Φ”»κœθΥα“χ»ή“ΚΘ§…ζ≥…ΑΉ…Ϊ≥ΝΒμΓΘ
(1)”……œ ω Β―ιΩ…÷ΣΘ§Ρ≥Έό…Ϊ»ή“Κ“ΜΕ®Κ§”–ΒΡ»ή÷ ΈΣ___________________ΓΘ
(2)≤Ϋ÷ηΔώΥυΒΟ¬Υ“ΚB÷–ΒΡ―τάκΉ”ΈΣ____________Θ®–¥άκΉ”ΖϊΚ≈Θ©ΓΘ
(3)≤Ϋ÷ηΔώ÷–Θ§œρ¬Υ‘ϋA÷–Φ”»κΙΐΝΩœΓœθΥαΘ§ΑΉ…Ϊ≥ΝΒμ≤ΩΖ÷»ήΫβΘ§–¥≥ωΑΉ…Ϊ≥ΝΒμ≤ΩΖ÷»ήΫβΕ‘”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ________________________________ΓΘ
ΓΨ¥πΑΗΓΩNa2SO4 ΓΔMgCl2 Ba2+ΓΔH+ΓΔNa+ ![]()
ΓΨΫβΈωΓΩ
ΝρΥαΆ≠‘Ύ»ή“Κ÷–œ‘άΕ…ΪΘ§ΧΦΥαΗΤΡ―»ή”ΎΥ°Θ§ΧΦΥαΡΤΚΆ«β―θΜ·±ΒΖ¥”Π…ζ≥…»ή”ΎΥαΒΡΧΦΥα±Β≥ΝΒμΘ§ΝρΥαΡΤΚΆ«β―θΜ·±ΒΖ¥”Π…ζ≥…≤Μ»ή”ΎΥαΒΡΝρΥα±Β≥ΝΒμΘ§«β―θΗυάκΉ”ΚΆΟΨάκΉ”Ζ¥”ΠΜα…ζ≥…«β―θΜ·ΟΨ≥ΝΒμΓΔ«β―θΜ·ΟΨ≥ΝΒμ»ή”ΎΥαΘ§¬»άκΉ”ΚΆ“χάκΉ”Ζ¥”Π…ζ≥…¬»Μ·“χ≥ΝΒμΓΘ»Γ…ΌΝΩ‘≠Έό…Ϊ»ή“Κ”Ύ ‘Ιή÷–Θ§Φ”»κΙΐΝΩΒΡBaΘ®OHΘ©2»ή“ΚΘ§…ζ≥…ΑΉ…Ϊ≥ΝΒμΘ§Ιΐ¬ΥΘ§ΒΟΒΫ¬Υ‘ϋAΚΆ¬Υ“ΚBΘ§œρ¬Υ‘ϋA÷–Φ”»κΙΐΝΩœΓœθΥαΥαΘ§ΑΉ…Ϊ≥ΝΒμ≤ΩΖ÷»ήΫβΘ§ΈόΤχ≈ί≤ζ…ζΘ§Υυ“‘»ή“Κ÷–“ΜΕ®≤ΜΚ§ΝρΥαΆ≠ΓΔΧΦΥαΗΤΓΔΧΦΥαΡΤΘ§“ΜΕ®Κ§”–¬»Μ·ΟΨΓΔΝρΥαΡΤΘ§Ω…ΡήΚ§”–¬»Μ·ΡΤΘΜ»Γ≤Ϋ÷ηΔώ÷–ΒΡ¬Υ“ΚB”Ύ ‘Ιή÷–Θ§Φ”»κœθΥα“χ»ή“ΚΘ§…ζ≥…ΑΉ…Ϊ≥ΝΒμΘ§¬»Μ·ΟΨΜα“ΐ»κ¬»άκΉ”Θ§Υυ“‘÷ΛΟς≤ΜΡή‘≠Έό…Ϊ»ή“ΚΕ®Κ§”–¬»Μ·ΡΤΓΘ
Θ®1Θ©”……œ ω Β―ιΩ…÷ΣΘ§Ρ≥Έό…Ϊ»ή“Κ“ΜΕ®Κ§”–ΒΡ»ή÷ ΈΣNa2SO4ΓΔMgCl2ΘΜ
Θ®2Θ©≤Ϋ÷ηIΥυΒΟ¬Υ“ΚB÷–ΒΡ―τάκΉ”ΈΣBa2+ΓΔH+ΓΔNa+ΘΜ
Θ®3Θ©≤Ϋ÷ηΔώ÷–Θ§œρ¬Υ‘ϋA÷–Φ”»κΙΐΝΩœΓœθΥαΘ§ΑΉ…Ϊ≥ΝΒμ≤ΩΖ÷»ήΫβΘ§ΑΉ…Ϊ≥ΝΒμ≤ΩΖ÷»ήΫβΕ‘”ΠΒΡΖ¥”Π ««β―θΜ·ΟΨΚΆœθΥαΖ¥”Π…ζ≥…œθΥαΟΨΚΆΥ°Θ§Μ·―ßΖΫ≥Χ ΫΈΣΘΚMgΘ®OHΘ©2+2HNO3=MgΘ®NO3Θ©2+2H2OΓΘ
Ι ¥πΑΗΈΣΘΚΘ®1Θ©Na2SO4ΓΔMgCl2ΘΜ
Θ®2Θ©Ba2+ΓΔH+ΓΔNa+ΘΜ
Θ®3Θ©MgΘ®OHΘ©2+2HNO3=MgΘ®NO3Θ©2+2H2OΓΘ