题目内容
【题目】Na2CO3溶液显碱性,CuSO4溶液与Na2CO3溶液混合产生蓝绿色沉淀,以下是某小组同学对沉淀组成的探究。
(提出假设)假设1:沉淀为Cu(OH)2 假设2:沉淀为CuCO3 假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
(查阅资料)无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
已知:nCuCO3mCu(OH)2 受热易分解,生成CuO、CO2、H2O。CuCO3![]() CuO+CO2↑ ;Cu(OH)2
CuO+CO2↑ ;Cu(OH)2![]() CuO+H2O
CuO+H2O
(物质成分探究)步骤1:将所得悬浊液过滤,洗涤滤渣后晾干;
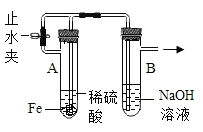
步骤2:甲同学取一定量上述蓝绿色固体,用如图装置(气密性良好)进行定性实验;
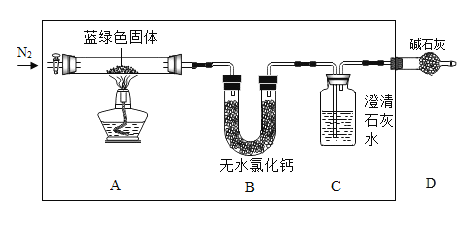
(1)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设_____成立。
(2)乙同学认为只要将图中B装置的试剂改用下列某试剂后,仅凭肉眼观察到的现象便可验证上述所有假设,该试剂是_____。
A 浓硫酸 B.无水硫酸铜 C 碱石灰 D 五氧化二磷
(物质含量探究)乙同学进一步探究假设3中固体的组成,用上述装置进行实验:若所取蓝绿色固体样品质量为54.2g置于A装置中,实验结束后装置B的质量增加5.4g,C中的产生沉淀的质量为20g。则该蓝绿色固体的化学式为_____。
【答案】1 B 2CuCO33Cu(OH)2
【解析】
(1)加热时,碳酸铜分解生成二氧化碳和黑色氧化铜,二氧化碳能使澄清的石灰水变浑浊,加热氢氧化铜时生成水蒸气和黑色氧化铜,水能使无水硫酸铜变蓝,若反应后A中蓝绿色固体变黑,C中无明显现象证明一定不含有碳酸铜,根据现象可知氢氧化铜,假设1正确,
(2)实验验证碳酸铜或氢氧化铜是利用受热分解生成的产物性质验证,加热时,碳酸铜分解生成二氧化碳和黑色氧化铜,加热氢氧化铜时生成水蒸气和黑色氧化铜,所以需要验证水的存在和二氧化碳的存在就可以证明产生的物质成分,装置A中可以观察加热是否变化为黑色固体,装置B选择无水硫酸铜验证是否生成水,澄清石灰水是否变浑浊证明是否生成二氧化碳。
物质含量探究:B中吸收的是水,水的质量=5.4g;C中的产生沉淀的质量为20g,则C中吸收的是二氧化碳生成碳酸钙白色沉淀,根据碳原子守恒得二氧化碳的质量为8.8g;氧化铜的质量=54.2g-5.4g-8.8g=40.0g,则氧化铜、水分子和二氧化碳的微粒个数之比=
![]() ,根据nCuCO3mCu(OH)2 受热易分解,生成CuO、CO2、H2O。CuCO3
,根据nCuCO3mCu(OH)2 受热易分解,生成CuO、CO2、H2O。CuCO3![]() CuO+CO2↑ ;Cu(OH)2
CuO+CO2↑ ;Cu(OH)2![]() CuO+H2O
CuO+H2O
所以其化学式为:2CuCO33Cu(OH)2。