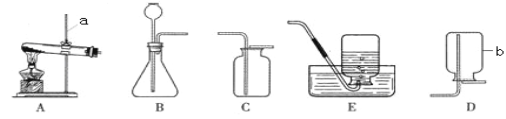
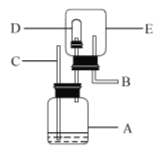
题目内容
【题目】亚硝酸钠(NaNO2)外形酷似食盐,误食会使人中毒。亚硝酸钠中氮元素的化合价为
A. +2 B. +3 C. +4 D. +5
【答案】B
【解析】试题分析:根据在化合物中,正负化合价的代数和为零,钠元素的化合价为+1,氧元素的化合价为-2,可得亚硝酸钠中氮元素的化合价为:(+1)+x+(-2)×2=0,解答x=+3;故答案选B.

【题目】(9分)废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如下图所示:
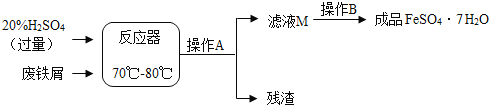
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有:,;
(2)滤液M中肯定含有的溶质的化学式是 、 ;
(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和 ;
(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4·7H2O)。已知硫酸亚铁的溶解度和析出晶体的组成如下表:
温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | ||||||||
根据溶解度表,硫酸亚铁晶体(FeSO4·7H2O)冷却结晶温度最高不超过 ℃;
(5)在化学反应中,若有元素化合价变化的反应定义为氧化还原反应。下列反应类型肯定是氧化还原反应的是 (填字母编号)。
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
硫酸亚铁晶体加强热会发生反应2FeSO4·7H2O 高温 Fe2O3+SO2+X+14H2O其生成物X的化学式
,该反应 (填“是”或“不是”)氧化还原反应。
【题目】(5分)a、b、c、d是初中化学中常见的4种元素,有关信息如下表所示。A、B、C、D、E是由上述4种元素中的一种或几种组成的纯净物。
元素 | a | b | c | d |
有关 信息 | 其单质A是密度最小的气体 | 地壳中含量最多的元素 | 形成化合物种类最多的元素 | 食盐中含有大量的该金属元素 |
(1)A的化学式是 。
(2) 单质B燃烧时,可生成不同的气体C或D。B充分燃烧生成C的化学方程式是 。
(3)E溶于水放出大量的热,得到溶质质量分数为10%的无色溶液Ⅰ,向Ⅰ中通入足量气体C后得溶液Ⅱ,发生反应的化学方程式是 ;与Ⅰ相比,Ⅱ中 (填序号)。
①溶质质量小 ②溶剂质量小 ③溶液质量大 ④溶质质量分数大