题目内容
 29、二氧化硫(SO2)的含量是空气质量监测的指标之一.请你参与兴趣小组对二氧化硫部分性质的实验探究.
29、二氧化硫(SO2)的含量是空气质量监测的指标之一.请你参与兴趣小组对二氧化硫部分性质的实验探究.(1)若雨水的pH小于5.6,表明空气受到污染.为了测定二氧化硫水溶液的pH,小明同学向一个集满二氧化硫气体的质地较软的塑料瓶中加入适量的水,立即旋紧瓶盖,振荡,使二氧化硫充分溶解(二氧化硫能与水反应形成亚硫酸)观察到的现象是
塑料瓶变瘪
;打开瓶塞,测定瓶中二氧化硫水溶液pH的实验操作是用玻璃棒蘸取溶液沾在pH试纸上,与标准比色卡比较颜色
.(2)为了探究二氧化硫能否与氢氧化钠反应,小宁同学用右图所示装置进行实验,发现试管内液面上升.小宁同学由此得到结论:二氧化硫能与氢氧化钠反应.你认为小宁同学由上述实验得出的结论是否合理?
否
(填“是”或“否”),理由是二氧化硫溶于水或与水反应均可有此现象
.分析:(1)气体二氧化硫溶于水、与水反应后,瓶内气体减少,瓶内压强减小,在外界大气压下塑料瓶会变形;测定溶液的pH时,可用玻璃棒把溶液沾在试纸上,通过与标准比色卡对比颜色而确定溶液的pH;
(2)图示的实验中出现试管内液面上升,说明气体减少,由于二氧化硫能溶于水、能与水反应、也能与氢氧化钠反应,因此仅凭气体减少判断二氧化硫与氢氧化钠发生了反应不够准确.
(2)图示的实验中出现试管内液面上升,说明气体减少,由于二氧化硫能溶于水、能与水反应、也能与氢氧化钠反应,因此仅凭气体减少判断二氧化硫与氢氧化钠发生了反应不够准确.
解答:解:(1)由于塑料瓶内的二氧化硫气体既能溶于水又能与水反应,因此加入水振荡后瓶内气体减少压强减小,在外界大气压作用下,塑料瓶会变瘪;测定溶液的pH的正确操作方法为:用玻璃棒蘸取溶液沾在pH试纸上,与标准比色卡比较颜色;
(2)氢氧化钠溶液为氢氧化钠溶于水所形成的混合物,倒扣入氢氧化钠溶液中的盛满二氧化硫气体的试管内液面上升,说明二氧化硫气体减少,但由于二氧化硫既能溶于水又能与水反应,并且也能与氢氧化钠反应,三个变化都会导致试管内气体减少,因此气体减少而液面上升不能证明二氧化硫与氢氧化钠发生了反应;
故答案为:
(1)塑料瓶变瘪;用玻璃棒蘸取溶液沾在pH试纸上,与标准比色卡比较颜色;
(2)否;二氧化硫溶于水或与水反应均可有此现象.
(2)氢氧化钠溶液为氢氧化钠溶于水所形成的混合物,倒扣入氢氧化钠溶液中的盛满二氧化硫气体的试管内液面上升,说明二氧化硫气体减少,但由于二氧化硫既能溶于水又能与水反应,并且也能与氢氧化钠反应,三个变化都会导致试管内气体减少,因此气体减少而液面上升不能证明二氧化硫与氢氧化钠发生了反应;
故答案为:
(1)塑料瓶变瘪;用玻璃棒蘸取溶液沾在pH试纸上,与标准比色卡比较颜色;
(2)否;二氧化硫溶于水或与水反应均可有此现象.
点评:变化的现象是变化本质的反映,但当一种现象受多种因素影响时,根据这种现象就不能简单的得出判断结论,此时可采取对比实验进行影响因素的探究.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标.某兴趣小组同学收集某地的雨水进行实验.
【相关信息】①每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
②SO2能使品红溶液褪色;
③pH<5.6的雨水为酸雨;
④海水呈弱碱性;
⑤BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
【分析讨论】①正常雨水的pH范围是:7>pH>5.6,偏酸性,这是因为 .
②酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于 .
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧化为H2SO4.试写出该反应的化学方程式 .
【提出猜想】同学们对刚收集到的酸雨样品中的溶质进行猜想:
猜想Ⅰ:酸雨中溶质只含有H2SO3;
猜想Ⅱ:酸雨中溶质只含有H2SO4;
猜想Ⅲ:酸雨中溶质 .
【实验探究】
(1)向刚收集的酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加 溶液,溶液呈 色.证明在酸雨样品中滴加的Ba(OH)2溶液已过量.
②向沉淀中加入足量盐酸,沉淀部分溶解且放出有刺激性气味气体.该反应的化学方程式为 ,根此现象有关酸雨中溶质的猜想 正确.
(2)某同学取酸雨样品V L,加入17.1%的Ba(OH)2溶液至不再产生沉淀时,恰好消耗10.00g Ba(OH)2溶液.该V L酸雨样品中溶解SO2的质量为 .
实验反思:在某些酸雨中还可分析出有硝酸存在,这是由于空气中含有某元素+4价氧化物的原因,这种氧化物的化学式为 .
拓展延伸:利用海水脱硫是减少SO2排放的有效方法,其工艺流程如下图所示:
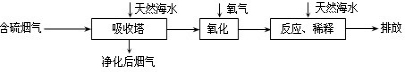
天然海水吸收了较多的含硫烟气后,有H2SO3生成,H2SO3与海水中的离子反应,会释放出CO2,通入氧气后氧化后,海水的酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单的实验方案: .
②氧化后的海水需要用大量的天然海水与之混合后才能排放,该操作的主要目的是 .
【相关信息】①每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
③pH<5.6的雨水为酸雨;
④海水呈弱碱性;
⑤BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
【分析讨论】①正常雨水的pH范围是:7>pH>5.6,偏酸性,这是因为
②酸雨能腐蚀金属制品,从基本反应类型上看主要反应属于
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧化为H2SO4.试写出该反应的化学方程式
【提出猜想】同学们对刚收集到的酸雨样品中的溶质进行猜想:
猜想Ⅰ:酸雨中溶质只含有H2SO3;
猜想Ⅱ:酸雨中溶质只含有H2SO4;
猜想Ⅲ:酸雨中溶质
【实验探究】
(1)向刚收集的酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加
②向沉淀中加入足量盐酸,沉淀部分溶解且放出有刺激性气味气体.该反应的化学方程式为
(2)某同学取酸雨样品V L,加入17.1%的Ba(OH)2溶液至不再产生沉淀时,恰好消耗10.00g Ba(OH)2溶液.该V L酸雨样品中溶解SO2的质量为
实验反思:在某些酸雨中还可分析出有硝酸存在,这是由于空气中含有某元素+4价氧化物的原因,这种氧化物的化学式为
拓展延伸:利用海水脱硫是减少SO2排放的有效方法,其工艺流程如下图所示:

天然海水吸收了较多的含硫烟气后,有H2SO3生成,H2SO3与海水中的离子反应,会释放出CO2,通入氧气后氧化后,海水的酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单的实验方案:
②氧化后的海水需要用大量的天然海水与之混合后才能排放,该操作的主要目的是
 二氧化硫(SO2)的含量是空气质量监测的指标之一.请你参与兴趣小组对二氧化硫部分性质的实验探究.
二氧化硫(SO2)的含量是空气质量监测的指标之一.请你参与兴趣小组对二氧化硫部分性质的实验探究.