题目内容
小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸钾、硫酸钠、硫酸镁溶液中的一种.小兵通过查阅资料得知:常温(20℃)下这三种物质的溶解度如下:| 物质 | K2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 1 3.0 | 1 9.0 | 36.0 |
(2)【提出假设】该溶液可能是______.
(3)【实验验证】
| 实验步骤 | 实验现象 | 实验结论 |
| ______ | ______ | ______ |

【答案】分析:(1)根据计算在该温度下,硫酸钾溶液的溶质的质量分数为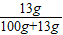 ×100%=11.5%,即最大浓度不会超过11.5%,而图中信息为15%,则一定不是硫酸钾溶液;
×100%=11.5%,即最大浓度不会超过11.5%,而图中信息为15%,则一定不是硫酸钾溶液;
(2)根据给出的试剂,可能是硫酸镁或硫酸钠溶液.
(3)根据硫酸钠或硫酸镁的化学性质来设计实验过程.
解答:解:(1)由物质在常温下的溶解度可知,硫酸钾溶液的溶质的质量分数为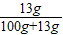 ×100%=11.5%,即最大浓度不会超过11.5%,
×100%=11.5%,即最大浓度不会超过11.5%,
故答案为:硫酸钾;因其在该温度下最大浓度不会超过11.5%;
(2)根据硫酸钠的溶解度,在该温度下,硫酸钠饱和溶液的溶质的质量分数为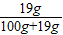 ×100%≈17%,即最大质量分数不会超过17%,
×100%≈17%,即最大质量分数不会超过17%,
根据硫酸镁的溶解度,在该温度下,硫酸镁饱和溶液的溶质的质量分数是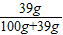 ×100%≈28.06%,即最大质量分数不会超过28.06%,
×100%≈28.06%,即最大质量分数不会超过28.06%,
由图中的标签可知,其质量分数为15.0%,则可能是硫酸钠,也可能是硫酸镁,
故答案为:硫酸钠,也可能是硫酸镁;
(3)因硫酸镁能与氢氧化钠反应生成白色沉淀,而硫酸钠不与氢氧化钠反应,则可利用氢氧化钠来验证无色试剂,
实验步骤为:取适量的溶液于试管中,滴加NaOH溶液;
实验现象为:溶液变浑浊,有白色沉淀生成(或无现象);
实验结论为:此溶液为硫酸镁溶液(或溶液为硫酸钠溶液);
故答案为:取适量的溶液于试管中,滴加NaOH溶液;溶液变浑浊,有白色沉淀生成(或无现象);此溶液为硫酸镁溶液(或溶液为硫酸钠溶液).
点评:本题考查缺失标签的药品成分的探究,属于开放性习题,能较好的考查学生的实验探究能力,不仅要求通过溶解度计算质量分数来猜测成分,还要求实验设计过程,训练学生思维,体现学生应用知识知识解决问题的能力.
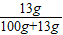 ×100%=11.5%,即最大浓度不会超过11.5%,而图中信息为15%,则一定不是硫酸钾溶液;
×100%=11.5%,即最大浓度不会超过11.5%,而图中信息为15%,则一定不是硫酸钾溶液;(2)根据给出的试剂,可能是硫酸镁或硫酸钠溶液.
(3)根据硫酸钠或硫酸镁的化学性质来设计实验过程.
解答:解:(1)由物质在常温下的溶解度可知,硫酸钾溶液的溶质的质量分数为
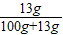 ×100%=11.5%,即最大浓度不会超过11.5%,
×100%=11.5%,即最大浓度不会超过11.5%,故答案为:硫酸钾;因其在该温度下最大浓度不会超过11.5%;
(2)根据硫酸钠的溶解度,在该温度下,硫酸钠饱和溶液的溶质的质量分数为
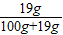 ×100%≈17%,即最大质量分数不会超过17%,
×100%≈17%,即最大质量分数不会超过17%,根据硫酸镁的溶解度,在该温度下,硫酸镁饱和溶液的溶质的质量分数是
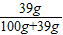 ×100%≈28.06%,即最大质量分数不会超过28.06%,
×100%≈28.06%,即最大质量分数不会超过28.06%,由图中的标签可知,其质量分数为15.0%,则可能是硫酸钠,也可能是硫酸镁,
故答案为:硫酸钠,也可能是硫酸镁;
(3)因硫酸镁能与氢氧化钠反应生成白色沉淀,而硫酸钠不与氢氧化钠反应,则可利用氢氧化钠来验证无色试剂,
实验步骤为:取适量的溶液于试管中,滴加NaOH溶液;
实验现象为:溶液变浑浊,有白色沉淀生成(或无现象);
实验结论为:此溶液为硫酸镁溶液(或溶液为硫酸钠溶液);
故答案为:取适量的溶液于试管中,滴加NaOH溶液;溶液变浑浊,有白色沉淀生成(或无现象);此溶液为硫酸镁溶液(或溶液为硫酸钠溶液).
点评:本题考查缺失标签的药品成分的探究,属于开放性习题,能较好的考查学生的实验探究能力,不仅要求通过溶解度计算质量分数来猜测成分,还要求实验设计过程,训练学生思维,体现学生应用知识知识解决问题的能力.

练习册系列答案
相关题目
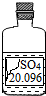
小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小兵同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
小兵同学根据上述信息.分析认为此溶液一定不是______溶液.为确定其成分,该同学对此溶液进行如下实验探究:
该溶液可能是______.
| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
该溶液可能是______.
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |

小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小兵同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
小兵同学根据上述信息.分析认为此溶液一定不是______溶液.为确定其成分,该同学对此溶液进行如下实验探究:
该溶液可能是______.

| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
该溶液可能是______.
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |

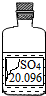 小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小兵同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种.小兵同学通过查阅资料得知,常温下这三种物质的溶解度如下表: (2009?湘西州)小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸钾、硫酸钠、硫酸镁溶液中的一种.小兵通过查阅资料得知:常温(20℃)下这三种物质的溶解度如下:
(2009?湘西州)小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损(如右图所示).老师告诉他,这瓶试剂可能是硫酸钾、硫酸钠、硫酸镁溶液中的一种.小兵通过查阅资料得知:常温(20℃)下这三种物质的溶解度如下: