��Ŀ����
����Ŀ����1�����Ƽ����¡����Ϸ�չ������شٽ����������Ľ�����
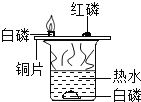
��������������ĸ�ķ��۾�����Ŀ�����������캽ĸ����Ҫ���ϣ�����������е�ˮ��____________�ȷ�����Ӧ����ʴ�������о�һ�ַ�ֹ������ʴ�ķ���_______________��
�ڿɽ������ϵ��������ȷ���������ּ���������ɫ��Ⱦ������������_____���ϣ����������������ϳ�������
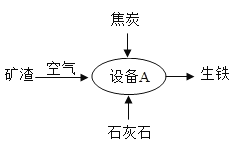
������������������ʯ�з����������ʯ����Ҫ�ɷ��� Fe2SiO4�����������������в�������̫����� Ar��36��Ar��38�������ʯ����Ԫ�صĻ��ϼ���______��Ar��36 �� Ar��38 ��ԭ�ӹ������ϵIJ�ͬ����_____��
���ڷ�ͥҽѧ�����ϳ��������鷨��֤���ܺ����Ƿ�Ϊ��˪��As2O3���ж�����п�����������������һ��������������˪���ͻᷢ����Ӧ�����黯�⣨AsH3�����Ȼ�п��ˮ��д���÷�Ӧ�Ļ�ѧ����ʽ_____
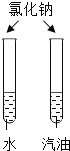
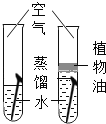
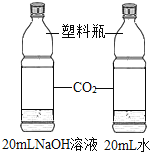
��2����ͼ������������������Ϊ 10%�� NaCl ��Һ��ʵ�����ʾ��ͼ��
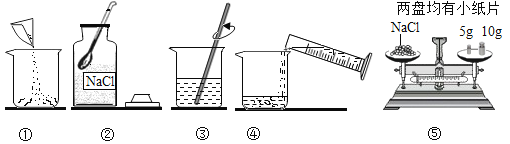
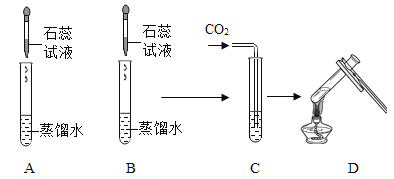
������ͼ��ʾ���ţ���ʾ������Һ����ȷ����˳��_____��
�ڳ��� NaCl ʱ����ƽƽ����״̬��ͼ����ʾ��������ʾ����ͼ�����ȡ�� NaCl ����Ϊ__________________
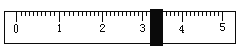
�۸��ݼ�����Ҫ��ȡˮ�������______ˮ���ܶ�Ϊ 1g/mL����
�ܳ��� NaCl ������ϷŻ�����ʱ��������һ������ȱ����һ��С�ǣ�����������������ȷ����������Һ��������������_____����������������С����������������10%��
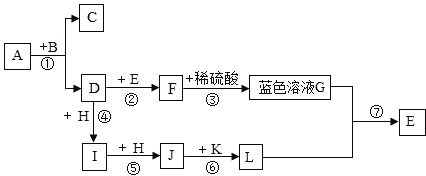
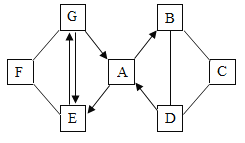
��3����ͼ��ʾijЩ���ʼ�ת����ϵ����Ӧ�����Ͳ��ֲ�����ʡ�ԣ���������A��C ������ͬԪ����ɵ���ɫҺ�壮��A ��������ɱ�����ã�D��I��J ��Ϊ��ɫ���壬���� I ��ʹ�����ʯ��ˮ����ǣ�K Ϊ����ɫ��ĩ����ش��������⣺
�ٷ�Ӧ���� B ���ʵ�������_____��
��ͼ�б���ķ�Ӧ�ٵ������ǻ��Ϸ�Ӧ����_____����������ţ���
����ͼ�б���� 12 �������У�������_____�֡�
�ܷ�Ӧ���е�����Ϊ_____��
��д����Ӧ�ߵĻ�ѧ����ʽ_____��
���𰸡����� ˢ���ᣨ���ֱ���Ľྻ��� �ϳ� +2 ��������ͬ As2O3+6Zn+12HCl=2AsH3+6ZnCl2+3H2O �ڢݢ٢ܢ� 18.2g 163.8mL С�� ������ �ڢܢ� 4 ��ɫ�����ɺ�ɫ Fe+CuSO4=Cu+FeSO4
��������
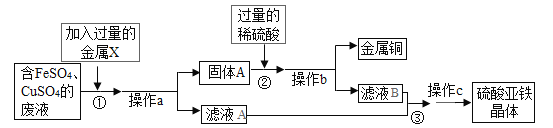
��3��������A��C ������ͬԪ����ɵ���ɫҺ�壬��A ��������ɱ�����ã�����AΪ�������⣬BΪ�������̣�CΪˮ��DΪ����������I ��ʹ�����ʯ��ˮ����ǣ���IΪ������̼��JΪ��ɫ���壬��J����I��������̼����H��Ӧ���ɣ�����HΪ̼��JΪһ����̼��K Ϊ����ɫ��ĩ������J��һ����̼����Ӧ������KΪ��������LΪ������ɫ��ҺGӦΪ����ͭ��Һ��F��D����������E��Ӧ���ɣ�������ϡ���ᷴӦ��������ͭ������FΪ����ͭ����EΪͭ��
��1���ٸ�����ʴ����������е�ˮ��������ͬ��Ӧ�Ľ��������������
��ֹ������ʴ�����ڸ���������Ӵ��������ø���㣬��ˢ���ᣬ�ֱ���Ľྻ�������ˢ���ᣨ���ֱ���Ľྻ�����
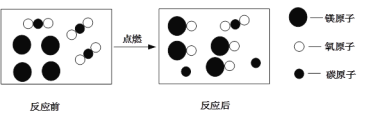
�����������л��ϳɲ��ϣ�����ϳɡ�
�����������Ļ��ϼ�Ϊx�����ݻ������и�Ԫ�صĻ��ϼ۵Ĵ�����Ϊ�㣬��x��2+��+4��+��-2����4=0��x=+2������+2��
Ar��36 �� Ar��38����ͬһ��Ԫ�أ���������ͬ�����ԭ��������ͬ�������ԭ������=������+������������Ar��36 �� Ar��38 ��ԭ�ӹ������ϵIJ�ͬ������������ͬ��������������ͬ��
����˪��п�����ᷴӦ�����黯�⡢�Ȼ�п��ˮ���ʷ�Ӧ�Ļ�ѧ����ʽдΪ��As2O3+6Zn+12HCl=2AsH3+6ZnCl2+3H2O��
��2��������һ�����������������Ȼ�����Һ�IJ����dz�ȡһ���������Ȼ��ƹ��壬���ƺõ��Ȼ��ƹ��嵹���ձ��У��ٽ���ȡ�õ�ˮ����ʢ���Ȼ��ƹ�����ձ��У�Ȼ���ò���������ӿ��Ȼ��ƹ�����ܽ⣬���ڢݢ٢ܢۣ�����ڢݢ٢ܢۡ�
�ڳ����Ȼ����õ�1��5g�����룬1��10g�����룬�����ʾ��Ϊ3.2g�����ȡ�� NaCl ����Ϊ18.2g������18.2g��
������ɿ�֪��������Һ��������������Ϊ10%����Һ������Ϊ18.2g��10%=182g����Ҫˮ������Ϊ182g18.2g=163.8g����ˮ�����Ϊ163.8g��1g/mL=163.8mL������163.8mL��
�ܳ��� NaCl �����Ĺ����У�һ������ȱ����һ��С�ǣ���ȡ���Ȼ��Ƶ�������С��18.2g����������Һ����������������С��10%������С�ڡ�
��3�����ɷ�����֪��BΪ�������̣��ڹ�������ֽ�ķ�Ӧ����������������ã���������á�
���ɷ�����֪�����ڻ��Ϸ�Ӧ���Ǣ�������ͭ��Ӧ��������ͭ����������̼��Ӧ���ɶ�����̼���ݶ�����̼��̼��Ӧ����һ����̼������ڢܢݡ�
���ɷ�����֪�����ڵ��ʵ�������D����������E��ͭ����H��̼����L������4�֣�����4.
�ܷ�Ӧ����ͭ�������ڼ��ȵ������·�Ӧ��������ͭ����Ӧ�й۲쵽������Ϊ��ɫ�����ɺ�ɫ�������ɫ�����ɺ�ɫ��
���ɷ�����֪����Ӧ������������ͭ��Ӧ��������������ͭ���ʷ�Ӧ�Ļ�ѧ����ʽдΪ��Fe+CuSO4=Cu+FeSO4��