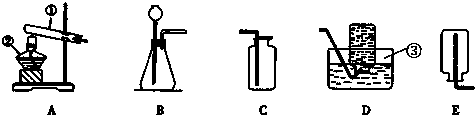题目内容
实验室把氯酸钾和二氧化锰的混合物30g装入大试管,加热制氧气.待反应完全后,冷却,称得固体残留物的质量为20.4g.求:(1)制得氧气的质量是多少?
(2)原混合物氯酸钾的质量是多少?
(3)若把该反应的固体残留物溶于水中,滤去不溶物后,取该滤液质量的1/10,与34g硝酸银溶液恰好完全反应,求该硝酸银溶液的溶质质量分数.
【答案】分析:(1)根据质量守恒定律可知,试管内物质质量的减少量就是生成的氧气的质量;
(2)根据氯酸钾分解的方程式,由氧气的质量可以计算出参加反应的氯酸钾及生成氯化钾的质量;
(3)根据氯化钾与硝酸银反应的方程式,由氯化钾的质量可求出硝酸银的质量,再根据质量分数的公式可求出该硝酸银溶液的溶质质量分数.
解答:解:(1)由题意可知,由于是完全反应,根据质量守恒,减少的质量就是生成的氧气的质量,即制得氧气:30g-20.4g=9.6g.
(2)设原混合物氯酸钾的质量为x,生成的氯化钾的质量为y
2KClO3 2KCl+3O2↑
2KCl+3O2↑
245 149 96
X y 9.6g
 解得:X=24.5g
解得:X=24.5g
 解得:y=14.9g
解得:y=14.9g
(3)由题意及溶液的均一性可知,滤液中氯化钾的质量为14.9g× =1.49g
=1.49g
设硝酸银溶液的溶质质量为Z
KCl+AgNO3═AgCl↓+KNO3
149 170
1.49g Z
 解得:Z=1.7g
解得:Z=1.7g
硝酸银溶液的溶质质量分数为: ×100%=5%
×100%=5%
答:(1)制得氧气的质量是9.6g;(2)原混合物氯酸钾的质量是24.5g;(3)该硝酸银溶液的溶质质量分数是5%.
点评:做本题的关键是要分析出试管内质量的减少量就是生成的氧气质量,再根据氧气质量进行进一步计算.
(2)根据氯酸钾分解的方程式,由氧气的质量可以计算出参加反应的氯酸钾及生成氯化钾的质量;
(3)根据氯化钾与硝酸银反应的方程式,由氯化钾的质量可求出硝酸银的质量,再根据质量分数的公式可求出该硝酸银溶液的溶质质量分数.
解答:解:(1)由题意可知,由于是完全反应,根据质量守恒,减少的质量就是生成的氧气的质量,即制得氧气:30g-20.4g=9.6g.
(2)设原混合物氯酸钾的质量为x,生成的氯化钾的质量为y
2KClO3
 2KCl+3O2↑
2KCl+3O2↑245 149 96
X y 9.6g
 解得:X=24.5g
解得:X=24.5g 解得:y=14.9g
解得:y=14.9g(3)由题意及溶液的均一性可知,滤液中氯化钾的质量为14.9g×
 =1.49g
=1.49g设硝酸银溶液的溶质质量为Z
KCl+AgNO3═AgCl↓+KNO3
149 170
1.49g Z
 解得:Z=1.7g
解得:Z=1.7g硝酸银溶液的溶质质量分数为:
 ×100%=5%
×100%=5%答:(1)制得氧气的质量是9.6g;(2)原混合物氯酸钾的质量是24.5g;(3)该硝酸银溶液的溶质质量分数是5%.
点评:做本题的关键是要分析出试管内质量的减少量就是生成的氧气质量,再根据氧气质量进行进一步计算.

练习册系列答案
相关题目
某化学兴趣小组的同学利用下列装置进行实验室制取气体的探究.请你参与探究并回答下列问题.

(1)完成下表:
如图:
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是 原因是: .
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是 (填写选项序号).
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当 停止加热.
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为 .请在装有所配制溶液的试剂瓶(如图)标签上标明相应信息.
④过滤、溶解、蒸发时都需用到的仪器是 (填序号);
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是 .

(1)完成下表:
| 气 体 | 药 品 | 装置组合 | 反应的化学方程式 |
| 氧 气 | 氯酸钾和二氧化锰 | ||
| 氢 气 | 稀盐酸与锌粒 | A、C | |
| 二氧化碳(干燥) | 大理石和稀盐酸 |
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为

④过滤、溶解、蒸发时都需用到的仪器是
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是