题目内容
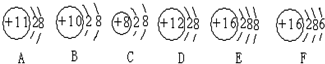 由下列结构图回答:
由下列结构图回答:(1)写出下列示意图的符号
A
D
(2)属于原子的是
(3)图F表示
(4)最外电子层未达到稳定结构的是
分析:(1)由各粒子的核内质子数确定元素种类,由核内质子数和核外电子数确定粒子所带电荷数,写出其离子符号或原子符号即可.
(2)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
(3)原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
(4)若粒子的最外层电子数为8,属于相对稳定结构.
(2)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
(3)原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
(4)若粒子的最外层电子数为8,属于相对稳定结构.
解答:解:(1)A质子数=11,核外电子数=10,质子数>核外电子数,为钠离子,其离子符号为:Na+.
B质子数=核外电子数=10,为氖原子,其原子符号为:Ne.
C质子数=8,核外电子数=10,质子数<核外电子数,为氧离子,其离子符号为:O2-.
D质子数=12,核外电子数=10,质子数>核外电子数,为镁离子,其离子符号为:Mg2+.
E质子数=16,核外电子数=18,质子数<核外电子数,为硫离子,其离子符号为:S2-.
F质子数=核外电子数=16,为硫原子,其原子符号为:S.
(2)BF质子数=核外电子数,均为原子;AD粒子的质子数>核外电子数,均为阳离子.
(3)图F中核内质子数为16,为硫元素,最外层电子数是6,大于4,在化学反应中易得到2个电子而形成阴离子.
(4)若粒子的最外层电子数为8,属于相对稳定结构,F粒子的最外层电子数是6,最外电子层未达到稳定结构.
故答案为:(1)Na+;Ne;O2-;Mg2+;S2-;S;(2)BF;AD;(3)硫;得到;阴;(4)F.
B质子数=核外电子数=10,为氖原子,其原子符号为:Ne.
C质子数=8,核外电子数=10,质子数<核外电子数,为氧离子,其离子符号为:O2-.
D质子数=12,核外电子数=10,质子数>核外电子数,为镁离子,其离子符号为:Mg2+.
E质子数=16,核外电子数=18,质子数<核外电子数,为硫离子,其离子符号为:S2-.
F质子数=核外电子数=16,为硫原子,其原子符号为:S.
(2)BF质子数=核外电子数,均为原子;AD粒子的质子数>核外电子数,均为阳离子.
(3)图F中核内质子数为16,为硫元素,最外层电子数是6,大于4,在化学反应中易得到2个电子而形成阴离子.
(4)若粒子的最外层电子数为8,属于相对稳定结构,F粒子的最外层电子数是6,最外电子层未达到稳定结构.
故答案为:(1)Na+;Ne;O2-;Mg2+;S2-;S;(2)BF;AD;(3)硫;得到;阴;(4)F.
点评:本题难度不大,考查学生对粒子结构示意图及其意义的理解,了解粒子结构示意图的意义是正确解题的关键.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目

 “嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列短文并回答有关问题.
“嫦娥一号”是我国自主研制、成功发射的第一个月球探测器.“嫦娥一号”的成功发射,使全国人民欢欣鼓舞.请同学们阅读下列短文并回答有关问题.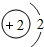 D.属于金属元素,在化学反应中易得到电子
D.属于金属元素,在化学反应中易得到电子