题目内容
【题目】(1)某同学用浓盐酸(溶质质量分数为37%)配制800 mL溶质质量分数为10%的稀盐酸。通过计算可知需要浓盐酸_____mL(精确到0.1mL)。
(2)某兴趣小组对石灰石样品进行如下实验取13g样品放入烧杯中,将80g稀盐酸分4记录如下。
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 10 | 7 | 4 | 3 |
请计算:
①样品中碳酸钙的质量_____。
②最终所得溶液中氯化钙的质量分数。_____(写出计算过程,最终结果保留0.1%)。
【答案】216.2 10g 解:根据表格可知,样品中碳酸钙的质量为10g,据此求算氯化钙的质量,
设最终所得溶液中氯化钙的质量为x,生成的二氧化碳的质量为y
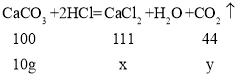
![]() =
=![]() =
=![]()
x=11.1g,y=4.4g,
最终所得溶液中氯化钙的质量分数是:![]() ×100%
×100%![]() 13.0%,
13.0%,
答:最终所得溶液中氯化钙的质量分数为13.0%
【解析】
(1)解:设需要浓盐酸的体积为V则:V×37%=800 mL×10%,解得![]() ;
;
(2)根据表格可知,样品中碳酸钙的质量为10g,据此求算氯化钙的质量,
设最终所得溶液中氯化钙的质量为x,生成的二氧化碳的质量为y
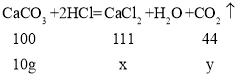
![]() =
=![]() =
=![]()
x=11.1g,y=4.4g,
最终所得溶液中氯化钙的质量分数是:![]() ×100%
×100%![]() 13.0%,
13.0%,
答:最终所得溶液中氯化钙的质量分数为13.0%

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目