题目内容
 根据如图判断,下列说法错误的是
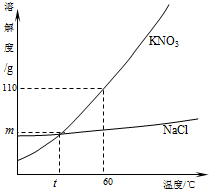
根据如图判断,下列说法错误的是
- A.NaCl和KNO3的溶解度都随温度升高而增大
- B.t℃时,KNO3和NaCl的溶解度相等
- C.60℃时,210克KNO3溶液蒸发可析出100g KNO3
- D.把KNO3中混有的少量NaCl分离出来可以用结晶法
C
分析:A、根据固体的溶解度曲线可知:两物质的溶解度受温度变化的影响的情况;
B、根据固体的溶解度曲线分析;
C、根据固体的溶解度曲线结合图中数据进行计算;
D、根据固体的溶解度曲线分析.
解答:A、由图可知,NaCl和KNO3的溶解度都随温度升高而增大,故A说法正确;
B、在t℃时,两物质的溶解度曲线交于一点,说明两物质的溶解度相等,故B说法正确;
C、60℃时,硝酸钾的溶解度是110g,因此210克KNO3溶液中含有110g硝酸钾固体,因此60℃时,210克KNO3溶液蒸发可析出110gKNO3固体,故C说法错误;
D、由于硝酸钾的溶解度随温度的升高而明显增大,而氯化钠的溶解度受温度的影响很小,因此可以通过降温结晶的方法将KNO3中混有的少量NaCl分离出来,故D说法正确.
故选C.
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义及根据固体的溶解度曲线来解决相关的问题.
分析:A、根据固体的溶解度曲线可知:两物质的溶解度受温度变化的影响的情况;
B、根据固体的溶解度曲线分析;
C、根据固体的溶解度曲线结合图中数据进行计算;
D、根据固体的溶解度曲线分析.
解答:A、由图可知,NaCl和KNO3的溶解度都随温度升高而增大,故A说法正确;
B、在t℃时,两物质的溶解度曲线交于一点,说明两物质的溶解度相等,故B说法正确;
C、60℃时,硝酸钾的溶解度是110g,因此210克KNO3溶液中含有110g硝酸钾固体,因此60℃时,210克KNO3溶液蒸发可析出110gKNO3固体,故C说法错误;
D、由于硝酸钾的溶解度随温度的升高而明显增大,而氯化钠的溶解度受温度的影响很小,因此可以通过降温结晶的方法将KNO3中混有的少量NaCl分离出来,故D说法正确.
故选C.
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义及根据固体的溶解度曲线来解决相关的问题.

练习册系列答案
相关题目
最近,中央电视台正在热播大型记录片《水问》,向人们说明了水是生命之源,万物之基,是人类最宝贵的自然资源,唤起人们关心水、爱护水、节约水的意识.
(1)我国规定水质必须在感官性指标、化学指标、病理学指标等方面.达标后方可以成为生活饮用水.各种指标的主要要求为:
a.不得呈现异色 b.不得有异嗅异味 c.水应澄清透明 d.不得含有细菌和病毒
①前两个指标可以利用 的吸附作用(填物质名称)而达到;
②自来水厂生产自来水的过程如下图所示:
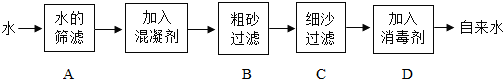
由上图可知净化水时,c、d两个指标可通过上图中的B、C、 过程而达到.
③水的硬度是一项重要的化学指标.日常生活中如何区分硬水与软水?请简述实验步骤与现象: .
(2)在化学反应中,水既可充当反应物也可充当生成物.下图表示几种化合物的相互转化关系,氧化物B为黑色固体、氧化物C为无色气体;E、D分别由三种元素组成,其中D能分解为C和H2O、E为白色难溶解于水的固体.
根据如图所示关系,回答下列问题:

①写出有关物质的化学式:C 、D 、E .
②写出反应b的文字(或化学式)表达式 .
(3)以下是某市水环境监测中心2007年10月发布的该市境内团结河三个不同河段水资源质量状况中的一部分内容:
①主要污染指标表述的文字中,涉及到的元素有N、 、 等 (写出两种元素符号即可).

②请你举出一种防止水体污染的措施: .
③氮肥的施用不当是水体中含氮量超标的原因之一.某生产化肥碳酸氢铵(NH4HCO3)的企业,作了一个如如图所示的大型户外广告.
根据相关信息计算:
Ⅰ.小明同学通过计算判断该广告属虚假广告,其理由是 .
Ⅱ.质量监督部门经过检测发现该化肥的含氮量为17.5%,则其中NH4HCO3的质量分数为 .
Ⅲ.列式计算:多少千克的硝酸铵(NH4NO3)和这袋化肥的含氮量相当? .
(1)我国规定水质必须在感官性指标、化学指标、病理学指标等方面.达标后方可以成为生活饮用水.各种指标的主要要求为:
a.不得呈现异色 b.不得有异嗅异味 c.水应澄清透明 d.不得含有细菌和病毒
①前两个指标可以利用
②自来水厂生产自来水的过程如下图所示:

由上图可知净化水时,c、d两个指标可通过上图中的B、C、
③水的硬度是一项重要的化学指标.日常生活中如何区分硬水与软水?请简述实验步骤与现象:
(2)在化学反应中,水既可充当反应物也可充当生成物.下图表示几种化合物的相互转化关系,氧化物B为黑色固体、氧化物C为无色气体;E、D分别由三种元素组成,其中D能分解为C和H2O、E为白色难溶解于水的固体.
根据如图所示关系,回答下列问题:

①写出有关物质的化学式:C
②写出反应b的文字(或化学式)表达式
| 河段编号 | 水质类别 | 主要污染指标 | 质量状况 |
| 甲 | Ⅱ | 良好 | |
| 乙 | Ⅳ | 汞 | 一般 |
| 丙 | 劣Ⅴ | 总磷、氨(NH3 )氮等 | 较差 |
①主要污染指标表述的文字中,涉及到的元素有N、

②请你举出一种防止水体污染的措施:
③氮肥的施用不当是水体中含氮量超标的原因之一.某生产化肥碳酸氢铵(NH4HCO3)的企业,作了一个如如图所示的大型户外广告.
根据相关信息计算:
Ⅰ.小明同学通过计算判断该广告属虚假广告,其理由是
Ⅱ.质量监督部门经过检测发现该化肥的含氮量为17.5%,则其中NH4HCO3的质量分数为
Ⅲ.列式计算:多少千克的硝酸铵(NH4NO3)和这袋化肥的含氮量相当?
(2008?泉州模拟)化学实验室开放日,小崖和小赳两同学在实验室中配制了如下四瓶溶液:饱和氢氧化钙溶液、饱和碳酸钠溶液、稀盐酸、氢氧化钠溶液,准备进行有关实验.过后发现未将饱和碳酸钠溶液和氢氧化钠溶液的试剂瓶贴上标签,并已混淆,两位同学决定将两瓶溶液鉴别出来.
[提出问题]仅从现有的氢氧化钙溶液和稀盐酸中选择合适的试剂就将饱和碳酸钠溶液和氢氧化钠溶液鉴别出来.
[假设]将混淆的两种溶液分别编号为A、B,假设A为碳酸钠溶液,B为氢氧化钠溶液.
[设计实验方案]两同学分别设计出如下的鉴别实验方案:
Ⅰ将两种溶液取样,分别滴入稀盐酸,根据是否有气泡产生判断各是哪种溶液.
Ⅱ将两种溶液取样,分别滴入饱和氢氧化钙溶液,振荡,根据是否有白色沉淀生成判断各是哪种溶液.
[进行实验]请你参与下列实验过程:
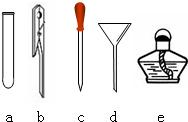
(1)在上述实验方案中选择方案______(填标号)进行实验;小崖指着实验桌上放置的实验仪器(如图所示)说:本实验不必用到的仪器是:______、______、______(填名称).同学们拿取所需仪器进行鉴别实验.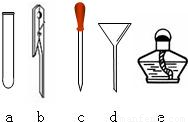
(2)同学间默契配合,边实验边填写如下实验报告:
(3)溶液鉴别完毕,同学们马上将两瓶溶液贴上标签,并检查一下四瓶溶液的瓶塞是否塞紧.小崖解释道:若无将试剂瓶口塞紧,某些溶液,如______溶液(选填一种溶液的溶质的名称)将与空气中的二氧化碳反应发生变质,这个反应的化学方程式是:______.
[提出问题]仅从现有的氢氧化钙溶液和稀盐酸中选择合适的试剂就将饱和碳酸钠溶液和氢氧化钠溶液鉴别出来.
[假设]将混淆的两种溶液分别编号为A、B,假设A为碳酸钠溶液,B为氢氧化钠溶液.
[设计实验方案]两同学分别设计出如下的鉴别实验方案:
Ⅰ将两种溶液取样,分别滴入稀盐酸,根据是否有气泡产生判断各是哪种溶液.
Ⅱ将两种溶液取样,分别滴入饱和氢氧化钙溶液,振荡,根据是否有白色沉淀生成判断各是哪种溶液.
[进行实验]请你参与下列实验过程:
(1)在上述实验方案中选择方案______(填标号)进行实验;小崖指着实验桌上放置的实验仪器(如图所示)说:本实验不必用到的仪器是:______、______、______(填名称).同学们拿取所需仪器进行鉴别实验.

(2)同学间默契配合,边实验边填写如下实验报告:
| 实验步骤 | 实验现象 | 结论、化学反应方程式 |
| ①______________________ ②______________________ | A溶液中样品中有_________ 产生 | 原假设________(填“正确”或“不正确”) 反应的化学反应方程式: ______________________ |

 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.

 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.
