题目内容
![]() 【题目】 根据下列装置图回答问题。
【题目】 根据下列装置图回答问题。
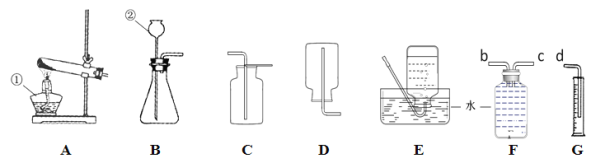
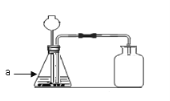
Ⅰ.写出仪器名称:① (19) ; ②(20) 。
Ⅱ.实验室用氯酸钾和二氧化锰的混合物制取氧气的化学方程式为 (21) ,制取并收集氧气的装置组合是(填字母) (22) 。用这套装置收集氧气时判断氧气已经集满的方法是 (23) 若通过排水法测定反应产生氧气的体积,各装置的连接顺序是:产生的O2 →b→c→d,请将F装置内的一根导管进行延伸、补画完整 (24) 。
Ⅲ.只能用D装置收集的气体应该具有的性质是 (25) 。
Ⅳ.若上述实验制得0.08g氧气,则分解的氯酸钾的物质的量为 (26) mol(根据化学方程式列式计算)。
【答案】(19)酒精灯;(20)长颈漏斗;(21)2KClO3 △![]() 2KCl+3O2↑;(22)AC(或者AE)(23)与(21)用带火星的木条(看到有大量气泡溢出);(24)将C端导管延长至接近瓶底;(25) 密度小于空气,能溶于水或与水发生反应。(26) 1/600 mol
2KCl+3O2↑;(22)AC(或者AE)(23)与(21)用带火星的木条(看到有大量气泡溢出);(24)将C端导管延长至接近瓶底;(25) 密度小于空气,能溶于水或与水发生反应。(26) 1/600 mol
【解析】
试题分析:根据所学知识可知Ⅰ.仪器名称:①为酒精灯,②为长颈漏斗;Ⅱ.实验室用氯酸钾和二氧化锰的混合物制取氧气的化学方程式为2KClO3 △![]() 2KCl+3O2↑,因为是固体加热制取气体,且气体的密度比空气大不易溶于水,故制取并收集氧气的装置组合是AC(或者AE),用这套装置收集氧气时判断氧气已经集满的方法是用带火星的木条(看到有大量气泡溢出),若通过排水法测定反应产生氧气的体积,各装置的连接顺序是:产生的O2 →b→c→d,F装置中的将C端导管延长至接近瓶底;,Ⅲ.只能用D装置收集的气体应该具有的性质是密度小于空气,能溶于水或与水发生反应,Ⅳ.
2KCl+3O2↑,因为是固体加热制取气体,且气体的密度比空气大不易溶于水,故制取并收集氧气的装置组合是AC(或者AE),用这套装置收集氧气时判断氧气已经集满的方法是用带火星的木条(看到有大量气泡溢出),若通过排水法测定反应产生氧气的体积,各装置的连接顺序是:产生的O2 →b→c→d,F装置中的将C端导管延长至接近瓶底;,Ⅲ.只能用D装置收集的气体应该具有的性质是密度小于空气,能溶于水或与水发生反应,Ⅳ.
解:制得氧气的物质的量为0.08/32=0.0025mol
设分解的氯酸钾的物质的量为Xmol
2KClO3 △![]() 2KCl+3O2↑
2KCl+3O2↑
2 3
X mol 0.0025mol
X=1/600 mol

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案