题目内容
 如图是某化学反应的微观示意图,相关分析正确的是( )
如图是某化学反应的微观示意图,相关分析正确的是( )分析:根据化学反应的微观示意图,分析反应物、生成物类别,根据反应的特点分析反应的类型.
解答: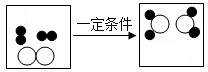 解:由化学反应的微观示意图,根据质量守恒定律可得出各物质的微粒间的反应数目关系:
解:由化学反应的微观示意图,根据质量守恒定律可得出各物质的微粒间的反应数目关系:
A、由上述各物质的微粒间的反应数目关系可知,该反应是两种单质反应生成一种化合物.故A分析不正确.
B、由上述各物质的微粒间的反应数目关系可知,参加反应的两种物质的物质的量之比为1:2.故B分析不正确.
C、由化学反应的微观示意图可知,该反应由两种物质生成了一种物质,属于化合反应.故C分析不正确.
D、由化学反应的微观示意图可知,构成生成物的分子是由两种不同的原子构成,若其中一种原子是氧原子.则该物质就是氧化物.故D分析正确.
故选D.
 解:由化学反应的微观示意图,根据质量守恒定律可得出各物质的微粒间的反应数目关系:
解:由化学反应的微观示意图,根据质量守恒定律可得出各物质的微粒间的反应数目关系:A、由上述各物质的微粒间的反应数目关系可知,该反应是两种单质反应生成一种化合物.故A分析不正确.
B、由上述各物质的微粒间的反应数目关系可知,参加反应的两种物质的物质的量之比为1:2.故B分析不正确.
C、由化学反应的微观示意图可知,该反应由两种物质生成了一种物质,属于化合反应.故C分析不正确.
D、由化学反应的微观示意图可知,构成生成物的分子是由两种不同的原子构成,若其中一种原子是氧原子.则该物质就是氧化物.故D分析正确.
故选D.
点评:读懂表示分子构成的模拟图,是解答问题的基础;同种原子构成的分子为单质分子,不同原子构成的分子为化合物分子.

练习册系列答案
相关题目
 26、日常用的干电池构造、组成如图1.某校化学活动小组进行的研究课题是《回收电池,变废为宝,保护环境》
26、日常用的干电池构造、组成如图1.某校化学活动小组进行的研究课题是《回收电池,变废为宝,保护环境》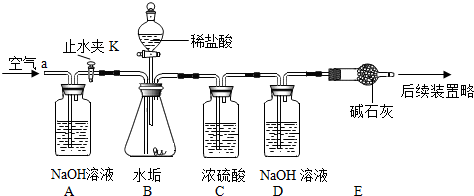
 某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,应逐渐减慢甚至停止.
某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,应逐渐减慢甚至停止.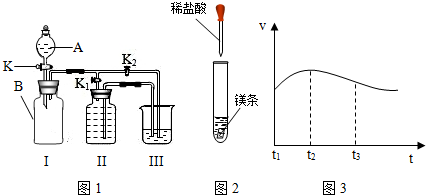
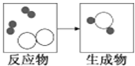 “见著知微”是化学学科的重要特点之一.如图是某化学反应的微观粒子示意图.
“见著知微”是化学学科的重要特点之一.如图是某化学反应的微观粒子示意图. B.两个
B.两个 C.一个
C.一个 D.两个
D.两个