题目内容
(1)从C、H、O、S、Cl、Na、N、Ca、Cu等9种元素中选择恰当的元素,用元素符号、化学式或化学方程式按下列要求填空:
①地壳中含量最多的元素______; ②造成硫酸型酸雨的气体______;③炉具清洁剂中的碱______; ④三种元素组成的有机物______.⑤生成两种非金属氧化物的分解反应______.⑥难溶性盐溶于盐酸的化学方程式______.
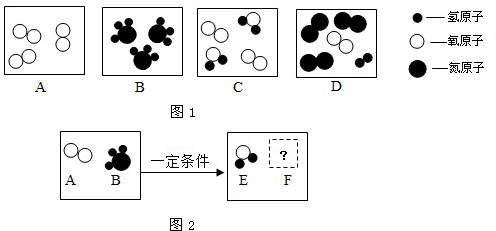
(2)A、B、C、D表示四种物质,其微观示意图如图1所示:
①从微观角度看,B图表示:3______(填化学符号)②从宏观角度看,图中表示混合物的是______(填字母符号)
(3)在一定的条件下,A和B能发生化学反应生成E和F,其微观示意图如图2所示:
①若F为空气中体积分数最大的气体,则该反应中生成的E和F的质量比______.
②若F为氧化物,且参加反应的A和B的分子个数比为5:4,则该反应的化学方程式为______.
解:(1)①地壳中含量比较多的前五种元素是:氧、硅、铝、铁、钙;故填O;
②造成硫酸型酸雨的气体为二氧化硫,根据读法,二氧化硫可表示为:SO2;
③炉具清洁剂含有氢氧化钠,钠元素是正一价,氢氧根是负一价,根据化合价原则,其化学式可表示为:NaOH;
④有机物是由碳元素组成的化合物,故由三种元素组成的有机物可表示为:C2H5OH;
⑤碳酸分解生成二氧化碳和水,二者都为氧化物,且反应为分解反应,反应的化学方程式为:H2CO3=CO2↑+H2O;
⑥由以上元素组成的难溶性盐为CaCO3或CuCO3,CaCO3与盐酸反应生成CaCl2、CO2和H2O,反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)由图示的情况可知:A中含有3个氧气的分子,B中含有的是3个氨气分子(NH3);由于C中含有2个水分子和2个氧气分子;D含有3个氮气分子和1个氢气分子1个氧气分子,所以C、D均是混合物,A是氧气的单质.故B图表示:3NH3;表示混合物的有CD;
(3)①F是氮气时其反应物是氧气与氨气,产物是水与氮气,其方程式是3O2+4NH3 6H2O+2N2,则水与氮气的质量比=(6×18):(4×14)=27:14;
6H2O+2N2,则水与氮气的质量比=(6×18):(4×14)=27:14;
②依据质量守恒定律可知F一定是氮的氧化物,因AB的分子个数比5:4,进而写出方程式是5O2+4NH3 6H2O+4NO.
6H2O+4NO.
故答案为:(1)①O ②SO2 ③NaOH ④C2H5OH (合理均对)⑤H2CO3=CO2↑+H2O ⑥CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)①NH3 ②CD (3)①27:14 ②5O2+4NH3 6H2O+4NO;
6H2O+4NO;
分析:(1)根据地壳中含量比较多的前五种元素是:氧、硅、铝、铁、钙;造成硫酸型酸雨的气体是二氧化硫;炉具清洁剂含有氢氧化钠;有机物是由碳元素组成的化合物;碳酸分解生成二氧化碳和水,二者都为氧化物,且反应为分解反应;由以上元素组成的难溶性盐为CaCO3或CuCO3.
(2)①利用图示中有关的物质的分子结构的知识对微粒的个数以及对分子的结构进行分析;
②混合物含有多种分子.
(3)①F是氮气时其反应物是氧气与氨气,产物是水与氮气,可书写出化学反应方程式,并对生成物的质量关系进行计算;
②依据质量守恒定律可知F一定是氮的氧化物,用AB的分子个数比可确定其化学式,进而写出方程式.
点评:本题主要考查了依据特定的条件书写化学式和书写化学方程式,书写化学用语时一定要规范,准确.利用分子由原子构成,同种原子构成的分子为单质分子,不同种原子构成的分子为化合物分子,纯净物中只含一种分子,混合物含有多种分子分析解答即可.
②造成硫酸型酸雨的气体为二氧化硫,根据读法,二氧化硫可表示为:SO2;
③炉具清洁剂含有氢氧化钠,钠元素是正一价,氢氧根是负一价,根据化合价原则,其化学式可表示为:NaOH;
④有机物是由碳元素组成的化合物,故由三种元素组成的有机物可表示为:C2H5OH;
⑤碳酸分解生成二氧化碳和水,二者都为氧化物,且反应为分解反应,反应的化学方程式为:H2CO3=CO2↑+H2O;
⑥由以上元素组成的难溶性盐为CaCO3或CuCO3,CaCO3与盐酸反应生成CaCl2、CO2和H2O,反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)由图示的情况可知:A中含有3个氧气的分子,B中含有的是3个氨气分子(NH3);由于C中含有2个水分子和2个氧气分子;D含有3个氮气分子和1个氢气分子1个氧气分子,所以C、D均是混合物,A是氧气的单质.故B图表示:3NH3;表示混合物的有CD;
(3)①F是氮气时其反应物是氧气与氨气,产物是水与氮气,其方程式是3O2+4NH3
 6H2O+2N2,则水与氮气的质量比=(6×18):(4×14)=27:14;
6H2O+2N2,则水与氮气的质量比=(6×18):(4×14)=27:14;②依据质量守恒定律可知F一定是氮的氧化物,因AB的分子个数比5:4,进而写出方程式是5O2+4NH3
 6H2O+4NO.
6H2O+4NO.故答案为:(1)①O ②SO2 ③NaOH ④C2H5OH (合理均对)⑤H2CO3=CO2↑+H2O ⑥CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)①NH3 ②CD (3)①27:14 ②5O2+4NH3
 6H2O+4NO;
6H2O+4NO;分析:(1)根据地壳中含量比较多的前五种元素是:氧、硅、铝、铁、钙;造成硫酸型酸雨的气体是二氧化硫;炉具清洁剂含有氢氧化钠;有机物是由碳元素组成的化合物;碳酸分解生成二氧化碳和水,二者都为氧化物,且反应为分解反应;由以上元素组成的难溶性盐为CaCO3或CuCO3.
(2)①利用图示中有关的物质的分子结构的知识对微粒的个数以及对分子的结构进行分析;
②混合物含有多种分子.
(3)①F是氮气时其反应物是氧气与氨气,产物是水与氮气,可书写出化学反应方程式,并对生成物的质量关系进行计算;
②依据质量守恒定律可知F一定是氮的氧化物,用AB的分子个数比可确定其化学式,进而写出方程式.
点评:本题主要考查了依据特定的条件书写化学式和书写化学方程式,书写化学用语时一定要规范,准确.利用分子由原子构成,同种原子构成的分子为单质分子,不同种原子构成的分子为化合物分子,纯净物中只含一种分子,混合物含有多种分子分析解答即可.

练习册系列答案
相关题目
