题目内容
【题目】工业上,利用溶液X(溶质为CuCl2和HCl)在50℃时与Cu反应制作电路。CuCl2消耗后,HCuCl2经处理又能转化为CuCl2,流程如图。下列说法错误的是( )
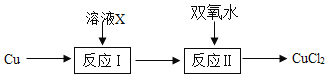
已知:①反应I CuCl2+Cu+2HCl=2HCuCl2
②反应Ⅱ2HCuC12+H2O2=2CuCl2+2H2O
A. 反应I和Ⅱ涉及的元素中仅Cu、O元素的化合价发生了变化
B. 反应Ⅱ中生成的CuCl2质量与溶液X中CuCl2质量一定相同
C. 工业上,每溶解6.4kg Cu时,外界只需提供34kg 10%的双氧水就能使生成的 HCuCl2全部转化为CuCl2
D. 若由Cu、CuCl、CuCl2中的若干种组成的10.66g混合物中,铜元素为6.4g,则该混合物中一定含CuCl2
【答案】B
【解析】
A、①反应I CuCl2+Cu+2HCl=2HCuCl2,是氯化铜中的铜元素化合价降低,单质铜中的铜化合价升高。反应Ⅱ 2HCuC12+H2O2=2CuCl2+2H2O中铜元素由反应前的+1变为反应后的+2,而氧元素由反应前的﹣1变为反应后的﹣2.所以反应I和Ⅱ涉及的元素中仅Cu、O元素的化合价发生了变化。选项A正确;
B、由于反应Ⅱ中生成的CuCl2质量是在溶液X中CuCl2质量基础上增加了加入的铜,所以一定不相同,生成的CuCl2质量质量增加了。选项B错误;
C、根据反应I CuCl2+Cu+2HCl=2HCuCl2和Ⅱ2HCuC12+H2O2=2CuCl2+2H2O可得关系式为 Cu~H2O2.设需要的10%的双氧水的质量为x
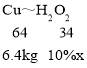
![]()
解得x=34kg。
选项C正确;
D、若由Cu、CuCl、CuCl2中的若干种组成的10.66g混合物中,铜元素为6.4g,即混合物中铜元素的质量分数为![]() ×100%≈60%,而CuCl中铜元素的质量分数为
×100%≈60%,而CuCl中铜元素的质量分数为![]() ×100%≈64.3%, CuCl2中铜元素的质量分数为
×100%≈64.3%, CuCl2中铜元素的质量分数为![]() ×100%≈47.4%,所以该混合物中一定含CuCl2。选项D正确。故选B。
×100%≈47.4%,所以该混合物中一定含CuCl2。选项D正确。故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列“课外实验”得出的结论错误的是
选项 | A | B | C | D |
课外 实验 |
|
|
|
|
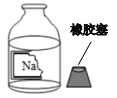
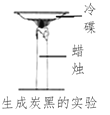
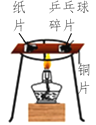
实验 结论 | 说明蜡烛 含有炭黑 | 说明有些花的色素 可做酸碱指示剂 | 不同物质着火点不同 | 说明同种溶质在不同种 溶剂里溶解性不同 |
A. AB. BC. CD. D