��Ŀ����
��1 ��С���ڹ���Ĵ�װ��Ƭ�з�����һ��С����������С��ɷ֣�CaO ��Fe �����ã������������������棺��ֹʳ�á���������˺��С������������Ĺ����ĩ���������غ�ɫ�ģ�������ǻҰ�ɫ�ġ���������������Ϊ�غ�ɫ��ĩ��Fe2O3���Ұ�ɫ��ĩӦ�ú���CaCO3��Fe ��Ϊ��֤�Լ����жϣ�С���������ʵ��̽��������һͬ���롣
��ʵ��Ŀ�ġ�֤ʵ�Ұ�ɫ��ĩ�к���CaCO3��Fe ��
���������ϡ����������л�ԭ�ԣ��ܶ�ȡijЩ�����������е�����ʹ������ԭ��
�ڰ�ɫ����ˮ����ͭ��ˮ�����ɫ��
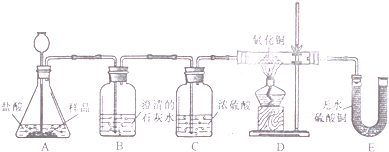
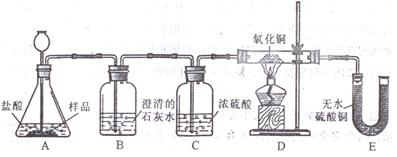
��ʵ����ơ�װ������ͼ��ʾ��
��ʵ��Ŀ�ġ�֤ʵ�Ұ�ɫ��ĩ�к���CaCO3��Fe ��
���������ϡ����������л�ԭ�ԣ��ܶ�ȡijЩ�����������е�����ʹ������ԭ��
�ڰ�ɫ����ˮ����ͭ��ˮ�����ɫ��
��ʵ����ơ�װ������ͼ��ʾ��
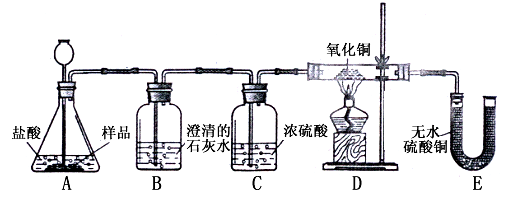
��ʵ��Ԥ���������
����Ҫ֤ʵ��Ʒ�к���CaCO3��B �й۲쵽��ʵ��������_____________________ ��B �з�����Ӧ�Ļ�ѧ����ʽΪ_____________________ ��
����Ҫ֤ʵ��Ʒ�к���Fe ��D ��Ӧ�۲쵽��ʵ��������________________________ ��E ��Ӧ�۲쵽��ʵ��������________________________ ��
�ۿ���С���ķ������ۣ���ͬѧ��ΪС���ڻҰ�ɫ��ĩ�л�Ӧ���б�����ʣ�����д������һ�����ʵĻ�ѧʽ__________________ ��
��С����Ϊ�غ�ɫ��ĩFe2O3Ҳ�������ᷴӦ������д����Ӧ�Ļ�ѧ����ʽ____ _______________________ ��
����Ҫ֤ʵ��Ʒ�к���CaCO3��B �й۲쵽��ʵ��������_____________________ ��B �з�����Ӧ�Ļ�ѧ����ʽΪ_____________________ ��
����Ҫ֤ʵ��Ʒ�к���Fe ��D ��Ӧ�۲쵽��ʵ��������________________________ ��E ��Ӧ�۲쵽��ʵ��������________________________ ��
�ۿ���С���ķ������ۣ���ͬѧ��ΪС���ڻҰ�ɫ��ĩ�л�Ӧ���б�����ʣ�����д������һ�����ʵĻ�ѧʽ__________________ ��
��С����Ϊ�غ�ɫ��ĩFe2O3Ҳ�������ᷴӦ������д����Ӧ�Ļ�ѧ����ʽ____ _______________________ ��
��2 ����ͭ��ͭ��п�Ͻ�������������������������������Ʒ��Ϊ�ⶨij��ͭ��ͭ��������������ȡ20g ����Ʒ���飬���뵽100g ϡ�����У�ǡ����ȫ��Ӧ����Ӧ�����ձ���ʣ�����������Ϊ119.6 �ˡ�
�ٷ�Ӧ����������������__________________ ��
�ڻ�ͭ��Ʒ��ͭ������������_______________ ��
�ۼ���ϡ���������ʵ�����������
�ٷ�Ӧ����������������__________________ ��
�ڻ�ͭ��Ʒ��ͭ������������_______________ ��
�ۼ���ϡ���������ʵ�����������
��1 ��
�ٳ���ʯ��ˮ����ǣ�Ca(OH)2+CO2=CaCO3��+H2O��
�ں�ɫ�����ɺ�ɫ����ɫ��������ɫ��
��CaO��Ca(OH)2��
��Fe2O3+6HCl=2FeCl3+3H2O��
��2 ��
��0.4g��
��35%��
�۽⣺��ϡ���������ʵ�����Ϊx
Zn + H2SO4 = ZnSO4 + H2��
98 2
x 0.4g
98:x=2:0.4g
��ã�x=19.6g
ϡ�����е����ʵ���������=19.6g/100g*100%=19.6%
��ϡ���������ʵ���������Ϊ19.6%
�ٳ���ʯ��ˮ����ǣ�Ca(OH)2+CO2=CaCO3��+H2O��
�ں�ɫ�����ɺ�ɫ����ɫ��������ɫ��
��CaO��Ca(OH)2��
��Fe2O3+6HCl=2FeCl3+3H2O��
��2 ��
��0.4g��
��35%��
�۽⣺��ϡ���������ʵ�����Ϊx
Zn + H2SO4 = ZnSO4 + H2��
98 2
x 0.4g
98:x=2:0.4g
��ã�x=19.6g
ϡ�����е����ʵ���������=19.6g/100g*100%=19.6%
��ϡ���������ʵ���������Ϊ19.6%

��ϰ��ϵ�д�
�����Ŀ