题目内容
【题目】实验室常用下列装置来制取 、收集气体。仪器 b 是分液漏斗,可通过旋转活塞分次 滴加液体。请回答以下问题.
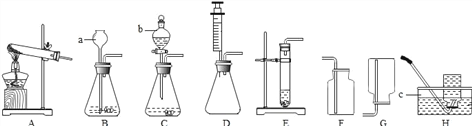
(1)仪器 a、c 的名称是:a_______________,c_______________。
(2)实验室用 KMnO4 制取 02,应选用的发生装置和收集装置的组合为_______________(填字 母序号),该发生装置的不足之处是_______________,该反应的化学方程式是_______________。
(3)实验室要制取少量 C02 应选择的较简单的发生装置是_______________(填字母序号),收 集二氧化碳的装置是_______________,用 H 装置_______________(填“能”或“否”)收集到二氧化碳。
(4)化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、 改进装置等途径来达到控制反应的目的。常温下块状电石(CaC2)与水反应生成乙炔 (C2H2) 气体和氢氧化钙,该反应的化学方程式是_______________,实验室制取乙炔时,须严格控制加水速 度,以免剧烈反应放热引起装置炸裂。图中适合制取乙炔气体的发生装置有_______________(填装 置序号)。
(5)某可燃性气体可能是乙炔、甲烷、一氧化碳中的一种或两种.已知 13g 该气体在足量 的氧气中充分燃烧生成 44g 二氧化碳和 9g 水,则该气体可能的组成为_______________。
A.乙炔
B.乙炔和一氧化碳的混合物
C.甲烷和一氧化碳的混合物
D.甲烷和乙炔的混合物.
(6)取 CaCl2 和 CaCO3 的混合物 12.5g 于烧杯中,向其中滴加足量的稀盐酸,滴加稀盐酸 的质量与产生气体质量的关系如图所示。求:反应结束后仪器内 CaCl2 的质量为_______________?(写出计算过程)

【答案】 长颈漏斗 水槽 AF 或 AH 试管口没有一团棉花 2KMnO4![]() K2MnO4+MnO2+O2↑ E F 能 CaC2+2H2O=Ca(OH)2+C2H2↑ C D AD 13.6g
K2MnO4+MnO2+O2↑ E F 能 CaC2+2H2O=Ca(OH)2+C2H2↑ C D AD 13.6g
【解析】(1)根据实验室常用仪器可知:a是长颈漏斗;c是水槽;(2)如果用高锰酸钾制氧气就需要加热,故选发生装置A,氧气不易溶于水,所以收集较为纯净的氧气可用排水法;氧气密度比空气大,可以用向上排空气法收集,所以制取装置为:AF 或 AH;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;反应方程式是: ![]()
![]()
![]() ;排水法收集满的方法是:集气瓶口有大气泡冒出;(3)实验室用大理石和盐酸反应制取二氧化碳,不需加热,属于固液常温型,故可选发生装置BCDE;制取少量CO2应选择的较简单的发生装置是E;二氧化碳密度比空气大,收集装置为F,二氧化碳能溶于水,但也不是无限制溶解,故用H装置也能收集到二氧化碳;(4)制取乙炔气体,是在常温下用块状电石与水反应,即固体和液体的反应;又因为该反应必须严格控制加水速度,免剧烈反应放热引起发生装置炸裂,所以应选用装置CD。D装置加液体的是注射器。可控制加水的速度。该反应的化学方程式是:
;排水法收集满的方法是:集气瓶口有大气泡冒出;(3)实验室用大理石和盐酸反应制取二氧化碳,不需加热,属于固液常温型,故可选发生装置BCDE;制取少量CO2应选择的较简单的发生装置是E;二氧化碳密度比空气大,收集装置为F,二氧化碳能溶于水,但也不是无限制溶解,故用H装置也能收集到二氧化碳;(4)制取乙炔气体,是在常温下用块状电石与水反应,即固体和液体的反应;又因为该反应必须严格控制加水速度,免剧烈反应放热引起发生装置炸裂,所以应选用装置CD。D装置加液体的是注射器。可控制加水的速度。该反应的化学方程式是: ![]() ;(5)已知13g该气体在足量的氧气中充分燃烧生成44g二氧化碳和9g水,根据质量守恒定律,需要氧气的质量为44g+9g-13g=40g,44gCO2中O元素的质量=
;(5)已知13g该气体在足量的氧气中充分燃烧生成44g二氧化碳和9g水,根据质量守恒定律,需要氧气的质量为44g+9g-13g=40g,44gCO2中O元素的质量=![]() ;9gH2O中O元素的质量=
;9gH2O中O元素的质量=![]() ,32g+8g=40g,说明混合气体中没有氧元素,则该气体可能的组成为乙炔或甲烷和乙炔的混合物;(6)由图可知,碳酸钙和100g稀盐酸反应生成了4.4g二氧化碳。设该石灰石样品中碳酸钙的质量为
,32g+8g=40g,说明混合气体中没有氧元素,则该气体可能的组成为乙炔或甲烷和乙炔的混合物;(6)由图可知,碳酸钙和100g稀盐酸反应生成了4.4g二氧化碳。设该石灰石样品中碳酸钙的质量为![]() ,生成氯化钙的质量为
,生成氯化钙的质量为![]()
![]()
100 111 44
![]()
![]() 4.4g
4.4g
![]()
![]() =10g
=10g
![]() =11.1g
=11.1g
原混合物中CaC2的质量为12.5g-10g=2.5g,所以反应结束后仪器内 CaCl2 的质量为2.5g+11.1g=13.6g。

 名校课堂系列答案
名校课堂系列答案