题目内容
除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
| 物 质 | 杂 质 | 试 剂 | 操 作 | |
| A | MgCl2溶液 | HCl | 过量Mg(OH)2 | 过滤 |
| B | CO2 | H2O | NaOH固体 | 干燥 |
| C | H2O | 悬浮物 | 明矾 | 吸附 |
| D | NaNO3溶液 | NaCl | 过量AgNO3溶液 | 过滤 |
| A、A | B、B | C、C | D、D |
考点:物质除杂或净化的探究,气体的干燥(除水),酸的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:A、HCl能与过量Mg(OH)2反应生成氯化镁和水,再过滤除去过滤的不溶于水的氢氧化镁,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、氢氧化钠固体具有吸水性,但能与二氧化碳反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、明矾溶于水生成的胶状物能对悬浮物进行吸附,对杂质沉降,但还需要进行过滤,故选项所采取的方法错误.
D、NaCl能与过量AgNO3溶液反应生成氯化银沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸银(过量的),不符合除杂原则,故选项所采取的方法错误.
故选:A.
B、氢氧化钠固体具有吸水性,但能与二氧化碳反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、明矾溶于水生成的胶状物能对悬浮物进行吸附,对杂质沉降,但还需要进行过滤,故选项所采取的方法错误.
D、NaCl能与过量AgNO3溶液反应生成氯化银沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸银(过量的),不符合除杂原则,故选项所采取的方法错误.
故选:A.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
有关说法错误的是( )
| A、除去镁粉中的铝粉可选用烧碱 |
| B、等质量Al分别与足量浓硫酸和足量浓NaOH溶液放出等量的H2 |
| C、铝分别与足量稀盐酸和NaOH溶液反应,当两个反应放出的气体体积相同时,消耗的HCl和NaOH物质的量比为3:1 |
| D、等质量的两份铝分别和等物质的量的H2SO4与NaOH反应,若生成氢气质量比为7:8,则可推断必定是酸中的铝过量,而碱过量 |
现有六种物质:铁粉、NaOH溶液、Ba(NO3)2溶液、稀硫酸、Fe2O3和CuSO4溶液.将它们两两混合后,能发生的化学反应共有( )
| A、7个 | B、6个 | C、5个 | D、4个 |
下列叙述正确的是( )
| A、若两种微粒的核外电子数相同,这两种微粒一定是同种元素 |
| B、若两种微粒的质子数相同,这两种微粒一定是同种元素 |
| C、若两种微粒只含一种元素,则这两种微粒的原子核中质子数一定相同 |
| D、若两种微粒是同种元素,这两种微粒的最外层电子数一定相同 |
下列叙述中,前者是化学性质后者是化学变化的( )
| A、通常状况下,氢气是无色、无味的气体;钢锭扎成钢条 |
| B、酒精易燃;食物变馊 |
| C、铁生锈;红磷燃烧 |
| D、硫酸具有腐蚀性;盐酸能与碱反应 |
人类的下列活动和行为不会造成江河湖水污染的是( )
| A、城市生活用水的任意排放 |
| B、农药、化肥的任意施用 |
| C、工业生产中“三废”的任意排放 |
| D、大量放养鱼虾 |
在日常生活中,下列做法正确的是( )
| A、用食盐水除去水壶内的水垢 |
| B、食醋显酸性,常用来除去餐具上的油污 |
| C、用碳酸钙做补钙剂 |
| D、用蒸馏的方法使硬水变为软水 |
下图为某反应的微观模拟示意图.从图中获得的有关信息不正确的是( )

| A、分子是化学变化中的最小粒子 |
| B、化学反应前后原子的数目没有增减 |
| C、该化学反应属于化合反应 |
| D、分子间存在一定的间隔 |
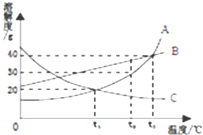 如图示是A、B、C三种固体物质的溶解度曲线.
如图示是A、B、C三种固体物质的溶解度曲线.