题目内容
向MgO和CuO的混合物12g中加入稀硫酸至恰好溶解,再向所得溶液中加入NaOH溶液至恰好沉淀完全,生成Mg(OH)2和Cu(OH)2沉淀的总质量为15.6g,则参加反应的NaOH的质量为
| A.3.6 g | B.8.0 g | C.16.0 g | D.18.0 g |
C
解析试题分析:根据关系式法:
因为MgO + H2SO4 ="===" MgSO4 +H2O
MgSO4 +2 NaOH ="===" Mg(OH)2↓ + Na2SO4
得到关系式MgO~MgSO4~2NaOH~Mg(OH)2,固体质量增加
40 80 58 18
因为CuO + H2SO4 ="===" CuSO4 +H2O
CuSO4 +2 NaOH ="===" Cu(OH)2↓ + Na2SO4
得到关系式CuO~CuSO4~2NaOH~Cu(OH)2,固体质量增加
80 80 98 18
即80份质量的NaOH参加反应时,固体质量增加18份,
设氢氧化钠的质量为x,可得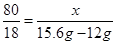 x =16g
x =16g
故选C
考点:根据化学方程式的计算

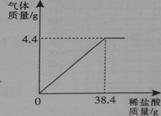
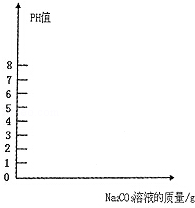
一包生石灰打开在空气中放置一段时间后,经测定固体成分为氢氧化钙和碳酸钙,向其中加入150g7.3%的稀盐酸恰好完全反应,同时生成2.2g二氧化碳。则固体混合物中钙、碳元素的质量比为………………………( )
| A.10:1 | B.5:1 | C.10:3 | D.20:3 |
向一定质量的硫酸铜溶液中加入不同质量的铁粉所呈现的信息如下表:
| Fe质量/g | 5.6 | 11.2 | 16.8 | 22.4[来 |
| Cu质量/g | 6.4 | 12.8 | 19.2 | 22.4 |

取一定量的氧化铁与氧化铜的混合物,加入溶质质量分数为9.8%的稀硫酸100g,恰好完全反应生成盐和水.原混合物中氧元素的质量是( )
| A.6.4g | B.3.2g | C.1.8g | D.1.6g |
(5分)铜镁合金常用作飞机天线等导电材料。欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金10g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下。请计算:
| 次 数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 8.5 | 7 | 6.6 | 6.6 |
(2)求所加稀硫酸中溶质的质量分数。(写出计算过程)