题目内容
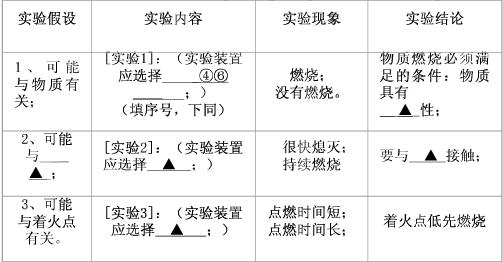
28、在日常生活中,燃烧现象屡见不鲜.你想过没有:发生燃烧的条件是什么?下面请你根据提供的物质设计实验来探究这一问题.
实验用品:酒精灯、蜡烛、玻璃杯、镊子、水、酒精、小木条、煤块、棉花球等.
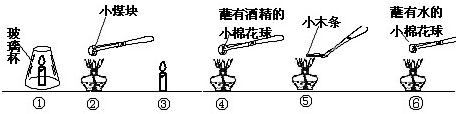
实验用品:酒精灯、蜡烛、玻璃杯、镊子、水、酒精、小木条、煤块、棉花球等.


分析:燃烧必须具备三个条件:一是要有可燃物;二是温度要达到可燃物的着火点;三是可燃物要与氧气接触.
解答:解:在探究有可燃物时,保持其它条件不变,选择一种可燃物和一种不是可燃物的.
本实验中选了酒精和水.实验二探究的是燃烧与氧气的关系,在探究时一种有充足的氧气,一种氧气量不足.
实验三探究温度与燃烧的关系,我们可选择一种温度高一种温度低的来验证.
故答案为:
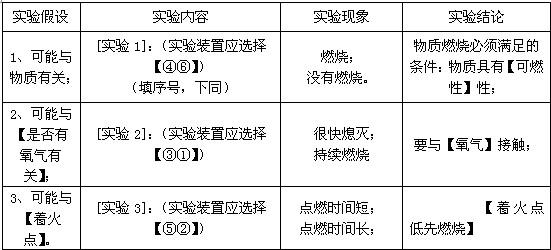
本实验中选了酒精和水.实验二探究的是燃烧与氧气的关系,在探究时一种有充足的氧气,一种氧气量不足.
实验三探究温度与燃烧的关系,我们可选择一种温度高一种温度低的来验证.
故答案为:

点评:在探究实验中,可选择对照实验,从对照实验中很容易就能得出所要的结果.

练习册系列答案
相关题目
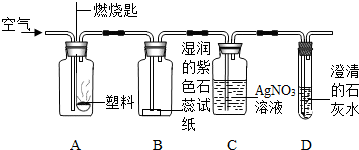


 日常生活中经常会用到蜡烛,为探究蜡烛的性质,现取一支普通照明用蜡烛进行下列实验:
日常生活中经常会用到蜡烛,为探究蜡烛的性质,现取一支普通照明用蜡烛进行下列实验: