题目内容
实验室的废液中含有氯化钙、盐酸、氯化镁和氯化铜,为从废液制得无水氯化钙,情趣小组的同学们设计了如下实验方案.
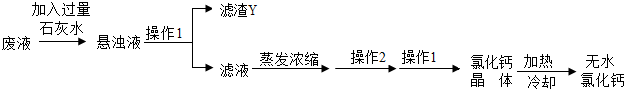
(1)分别写出操作Ⅰ和Ⅱ的名称: 、 .
(2)滤渣Y中含有 (填写化学式)
(3)加足量石灰水的作用是 ,写出其中属于中和反应的化学方程式: .

(1)分别写出操作Ⅰ和Ⅱ的名称:
(2)滤渣Y中含有
(3)加足量石灰水的作用是
考点:物质的相互转化和制备,过滤的原理、方法及其应用,蒸发与蒸馏操作,中和反应及其应用,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)分离不溶于水的固体的操作为过滤;蒸发浓缩后需要降温冷却,再进行过滤即可得到氯化钙晶体;
(2)考虑氯化镁和氯化铜与氢氧化钙的反应生成物;
(3)根据石灰水是为了除去盐酸、氯化镁、氯化铜,将它们转化为氯化钙考虑;根据中和反应的定义考虑中和反应方程式的书写;
(2)考虑氯化镁和氯化铜与氢氧化钙的反应生成物;
(3)根据石灰水是为了除去盐酸、氯化镁、氯化铜,将它们转化为氯化钙考虑;根据中和反应的定义考虑中和反应方程式的书写;
解答:解:
(1)分离不溶于水的固体的操作为过滤,故操作1为过滤;将滤液蒸发浓缩后再降温结晶,就会有氯化钙晶体析出,再进行过滤就能得到氯化钙,所以操作2的名称是降温结晶;
(2)滤渣是指的不溶于水的固体即沉淀,氯化镁和氯化铜与氢氧化钙反应生成的沉淀有氢氧化铜沉淀、氢氧化镁沉淀;故答案为:Mg(OH)2、Cu(OH)2
(3)加入石灰水就是为了和盐酸、氯化镁、氯化铜发生反应,将它们转化为氯化钙,所以加过量石灰水的作用是为了除尽盐酸、氯化镁和氯化铜;中和反应是酸和碱反应生成盐和水的反应,所以是氢氧化钙与盐酸反应生成氯化钙和水,用观察法配平,所以方程式是:Ca(OH)2+2HCl═CaCl2+2H2O;
故答案为:
(1)过滤;冷却结晶(或降温结晶);
(2)Mg(OH)2、Cu(OH)2;
(3)为了除尽盐酸、氯化镁和氯化铜;Ca(OH)2+2HCl═CaCl2+2H2O.
(1)分离不溶于水的固体的操作为过滤,故操作1为过滤;将滤液蒸发浓缩后再降温结晶,就会有氯化钙晶体析出,再进行过滤就能得到氯化钙,所以操作2的名称是降温结晶;
(2)滤渣是指的不溶于水的固体即沉淀,氯化镁和氯化铜与氢氧化钙反应生成的沉淀有氢氧化铜沉淀、氢氧化镁沉淀;故答案为:Mg(OH)2、Cu(OH)2
(3)加入石灰水就是为了和盐酸、氯化镁、氯化铜发生反应,将它们转化为氯化钙,所以加过量石灰水的作用是为了除尽盐酸、氯化镁和氯化铜;中和反应是酸和碱反应生成盐和水的反应,所以是氢氧化钙与盐酸反应生成氯化钙和水,用观察法配平,所以方程式是:Ca(OH)2+2HCl═CaCl2+2H2O;
故答案为:
(1)过滤;冷却结晶(或降温结晶);
(2)Mg(OH)2、Cu(OH)2;
(3)为了除尽盐酸、氯化镁和氯化铜;Ca(OH)2+2HCl═CaCl2+2H2O.
点评:解答本题关键是要知道方程式的书写方法,氢氧化钙与酸、盐都能反应,知道氢氧化铜、氢氧化镁都是沉淀,熟悉中和反应的特点.

练习册系列答案
相关题目
某水溶液中含有以下离子中的若干种:K+、Cl-、Ca2+、Zn2+、CO32-、SO42-,现取两份溶液各100mL分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有沉淀产生.根据上述实验,以下有关原溶液的论断不正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有沉淀产生.根据上述实验,以下有关原溶液的论断不正确的是( )
| A、Cl-一定存在 |
| B、CO32-和SO42-一定存在,且二者的个数比为1:2 |
| C、Zn2+ 和Ca2+一定不存在 |
| D、100mL溶液中K+的质量不小于2.34g |
实验室用98%的浓硫酸(密度1.84g/cm3)配制一定溶质质量分数的稀硫酸,不需要的仪器是( )
| A、玻璃棒 | B、量筒 |
| C、烧杯 | D、托盘天平 |