题目内容
【题目】氯化钙应用广泛,以石灰石(杂质主要是Fe2O3、MgSO4)为原料生产氯化钙的流程如下。
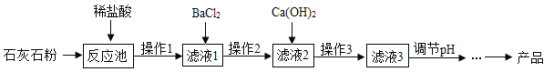
(1)石灰石研磨成粉末的目的是_______。
(2)滤液1中的溶质有HCl、MgSO4 、________。
(3)操作1、2、3中用到的玻璃仪器有玻璃棒、烧杯和_____。
(4)滤液3呈碱性,为使溶液pH降低,可加入适量的_______(选填序号)。
A 稀硫酸B NaOH溶液C 稀盐酸
【答案】使其充分反应,加快速率 CaCl2 、FeCl3 漏斗(或普通漏斗或三角漏斗) C
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,氧化铁和稀盐酸反应生成氯化铁和水。
(1)石灰石研磨成粉末,能增大和稀盐酸反应的接触面积,故石灰石研磨成粉末的目的是使其充分反应,加快速率。
(2)石灰石(杂质主要是Fe2O3、MgSO4),加入稀盐酸,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,氧化铁和稀盐酸反应生成氯化铁和水,故滤液1中的溶质有HCl、MgSO4 、CaCl2 、FeCl3。
(3)操作1、2、3是过滤操作,用到的玻璃仪器有玻璃棒、烧杯和漏斗。
(4)滤液3呈碱性,为使溶液pH降低,应该加酸性物质,加入稀硫酸会引入硫酸根杂质,加入稀盐酸和碱反应生成盐和水,没有引入新杂质,故选C。

 阅读快车系列答案
阅读快车系列答案【题目】有一瓶标签受损、没盖瓶盖且装有无色液体的试剂瓶,如图所示。
老师告诉大家,瓶内原有的液体只能是碳酸钠溶液、氢氧化钠溶液、氯化钠溶液、蒸馏水中的一种。为了判断瓶内是何种溶质,并确定试剂瓶的标签,化学小组的同学进行了如下探究活动。
![]()
(实验探究)
(1)从受损的标签信息看,大家一致认为该液体不可能是___________。
(2)甲同学设计了如下方案进行探究。
实验操作 | 实验现象 | 实验结论 |
取适量瓶内液体加入试管中,滴加足量的稀盐酸 | ________ | 该液体是碳酸钠溶液 |
(3)乙同学认为甲同学的结论不准确,又设计了如下方案进行探究。
实验操作 | 实验现象 | 实验结论 |
取适量瓶内液体加入试管中,滴加过量Ca(OH)2溶液。静置后,取上层清液,滴加酚酞溶液 | ________ | 该液体中的溶质为氢氧化钠和碳酸钠。反应的化学方程式:________ |
(4)丙同学认为乙同学的实验方案有不足之处, 于是丙同学只改用了一种与乙同学所加物质类别不同的溶液,重新按照乙的方法进行实验,得到的实验现象和结论与乙同学的完全一致,且结论完全正确。则丙同学改用的试剂为_______________。
(实验结论)实验结束后,最终得到的结论是:原试剂瓶标签_____________。
(反思与交流)
(1)为了不使标签破损,应如何正确操作_______________________。
(2)药品取完之后应及时密封保存。