题目内容
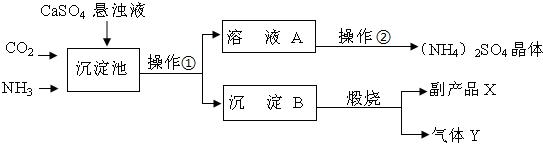
某实验小组根据查阅的资料对100 g含有泥沙、MgCl2的粗盐进行提纯。

(1)操作①、③的名称分别是 、 。
(2)溶液A中的溶质是 (写化学式)。
(3)溶液A与NaOH溶液反应生成Mg(OH)2固体的化学方程式为 。
(4)最后得到的NaCl固体的质量为__________ g。

(1)操作①、③的名称分别是 、 。
(2)溶液A中的溶质是 (写化学式)。
(3)溶液A与NaOH溶液反应生成Mg(OH)2固体的化学方程式为 。
(4)最后得到的NaCl固体的质量为__________ g。
(1)过滤 蒸发 (2)NaCl、MgCl2
(3)MgCl2 + 2NaOH ="===" Mg(OH)2↓+ 2NaCl (4)102.4
(3)MgCl2 + 2NaOH ="===" Mg(OH)2↓+ 2NaCl (4)102.4
试题分析:(1)根据混合物分离的方法分析,过滤可将不溶于液体的固体与液体分离开来,故操作①是过滤;而蒸发是将氯化钠溶液中的水分除去以得到溶质氯化钠晶体,故操作③是蒸发。
(2)根据题意,粗盐中含有氯化钠、泥沙和MgCl2,其中氯化钠和MgCl2易溶于水,而泥沙不溶于水,故溶液A的溶质是NaCl、MgCl2。
(3)MgCl2与NaOH溶液反应生成Mg(OH)2沉淀和氯化钠,故反应的化学方程式为MgCl2 + 2NaOH = Mg(OH)2↓+ 2NaCl。
(4)根据上面的分析可知,最后所得NaCl来自两部分,其一是原样品中的氯化钠,其二是反应生成的氯化钠。
设粗盐样品中含氯化镁的质量为x,同时生成氯化钠的质量为y
MgCl2 + 2NaOH = Mg(OH)2↓+ 2NaCl。
95 80 117
x 80g×20% y
95:80=x:80g×20% 80:117=80g×20%:y
解得x=19g y=23.4g
则最后得到的NaCl固体的质量=(100g-2g-19g)+23.4g=102.4g。
点评:解答本题的关键是,根据题意书写反应的化学方程式,然后依据已知量对未知的应求量进行求解计算即可,要注意的是最后得到的NaCl固体来自两部分,其一是原样品中的氯化钠,其二是反应生成的氯化钠。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目


 ,
, 。
。