题目内容
下列生产设计方案从原料到制取较纯的最终产物,理论上正确,操作上可行,经济上合理的是( )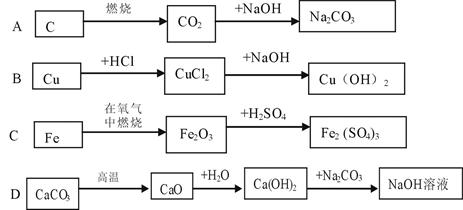

D
试题分析:A 较为耗能,而且氢氧化钠较贵,不合理;B 铜不和盐酸反应,不合理;C 铁在氧气中燃烧生成四氧化三铁,没有三氧化二铁生成,不合理;D 较为合理,经济上也可以接受。
点评:常见化学反应属于必考题型,但是考察形式比较多样,选择题中出现近年也比较多见,注意总结,记忆时注意细心。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
题目内容


 备战中考寒假系列答案
备战中考寒假系列答案