题目内容
某课外活动小组通过Internet网上资料得知:废弃的定影液中含有一定量的AgNO3.他们从摄影店收集到一些废弃的定影液,准备将其中的银以单质的形式全部回收.于是,他们进行了以下的实验活动:
(1)【设计方案】
①向定影液中加入比银活泼的金属单质
②除去金属混合物中的杂质,得到较纯的银单质
(2)【小组讨论】
①选择加入的金属
甲同学认为:向定影液中加入过量的铜粉,则得到的金属混合物含有银和铜;
乙同学认为:向定影液中加入过量的铁粉,则得到的金属混合物含有银和铁.
你认为哪位同学的方案更合理并说明理由?答:______.同学们最终选择了合理的方案,该方案反应的化学方程式为______.
②除去银粉中混有的金属:应向金属混合物中加入的试剂是______.
(3)【进行试验】过程如图:
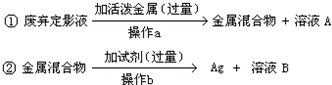
请问:溶液B中溶质的化学式为______.
(4)【产品证明】请你设计一个简单方法验证得到的银中是否含有加入的过量金属______.
解:(2)①铜、铁皆可置换出银,但铜、银都不与酸反应,而铁可与酸反应生成盐和氢气,且铜比铁的单价要高,故乙同学方案合理. 化学方程式为:Fe+2AgNO3=2Ag+Fe(NO3)2
②铁可与酸反应生成可溶亚铁盐和氢气,而银不与酸发生反应,因此选择稀盐酸.
(3)铁与硝酸银反应生成银和硝酸亚铁,得到的金属混合物为银和铁,加入过量盐酸,铁与盐酸反应生成氯化亚铁和氢气,因此溶液B中含有剩余的盐酸和氯化亚铁.
(4)由于铁粉能被磁铁吸引,可选用磁铁进行检验;或铁能与酸反应产生氢气,向金属粉末中滴加稀盐酸,观察是否有有气泡进行检验;
故答案为:(2)①乙. Fe+2AgNO3=2Ag+Fe(NO3)2.
②稀盐酸.
(3)HCl、FeCl2.
(4)用磁铁接触,观察银粉能否被吸引(或取少量银粉加入稀盐酸,看有无气泡放出);
分析:(2)根据金属活动性顺序,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来,排在氢之前的金属能与酸反应置换出氢气.要将废弃的定影液中的银以单质的形式回收,可采用活动性比银强的金属置换银.铁可与酸反应,而铜银都不与酸反应
(3)铁与硝酸银反应生成银和硝酸亚铁,得到的金属混合物为银和铁,加入过量盐酸,铁与盐酸反应生成氯化亚铁和氢气,由此判断溶液B中的溶质.
(4)根据铁与银性质差别,设计实验证明金属银的粉末中是否含有铁粉;
点评:本题考查了金属活动性顺序及应用、铁与盐酸的反应以及实验方案的比较.考查学生分析问题及运用知识解决问题的能力.
②铁可与酸反应生成可溶亚铁盐和氢气,而银不与酸发生反应,因此选择稀盐酸.
(3)铁与硝酸银反应生成银和硝酸亚铁,得到的金属混合物为银和铁,加入过量盐酸,铁与盐酸反应生成氯化亚铁和氢气,因此溶液B中含有剩余的盐酸和氯化亚铁.
(4)由于铁粉能被磁铁吸引,可选用磁铁进行检验;或铁能与酸反应产生氢气,向金属粉末中滴加稀盐酸,观察是否有有气泡进行检验;
故答案为:(2)①乙. Fe+2AgNO3=2Ag+Fe(NO3)2.
②稀盐酸.
(3)HCl、FeCl2.
(4)用磁铁接触,观察银粉能否被吸引(或取少量银粉加入稀盐酸,看有无气泡放出);
分析:(2)根据金属活动性顺序,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来,排在氢之前的金属能与酸反应置换出氢气.要将废弃的定影液中的银以单质的形式回收,可采用活动性比银强的金属置换银.铁可与酸反应,而铜银都不与酸反应
(3)铁与硝酸银反应生成银和硝酸亚铁,得到的金属混合物为银和铁,加入过量盐酸,铁与盐酸反应生成氯化亚铁和氢气,由此判断溶液B中的溶质.
(4)根据铁与银性质差别,设计实验证明金属银的粉末中是否含有铁粉;
点评:本题考查了金属活动性顺序及应用、铁与盐酸的反应以及实验方案的比较.考查学生分析问题及运用知识解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
二氧化硫是大气污染物之一,表一为我国环境空气质量标准中对每次空气质量测定中的S02最高浓度限值.

| S02最高浓度限值(单位mg?m-3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
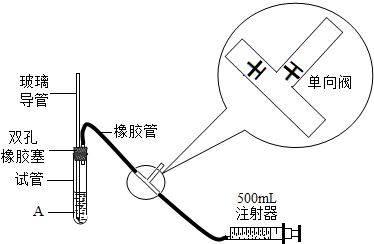
(1)检查装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端浸没在水中),然后向外轻轻拉动注射器的活塞时,将会看到________ (填写实验现象),则证明该装置的气密性良好.
(2)已知二氧化硫与碘水的反应为:SO2+I2+2H2O═H2SO4+2HI.向试管中加入1.0mL溶质质量分数为1.27×10-4的碘水( 此时溶液的密度与水的密度近似 ),用适量的蒸馏水稀释后再加入2~3滴无色淀粉溶液(遇到碘单质变蓝色),配制成溶液A.测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由________色变为________色时反应恰好完全进行.
(3)课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,分别测量化学实验室和教室的空气中的S02含量.当反应恰好完全进行,记录抽气次数如下(假设每次抽气500mL).请将表二填写完整(计算时保留二位有效数字).(I-127 S-32 O-16)
表二 不同组别的测量值
| 组 别 | 第一小组(实验室) | 第二小组(教室) |
| 抽气次数 | 110 | 150 |
| 空气中S02的含量(单位:mg?m-3) |
二氧化硫是大气污染物之一,表一为我国环境空气质量标准中对每次空气质量测定中的S02最高浓度限值.

国家环保总局规定从2005年1月1日起将各类实验室纳入环保监管范围.为粗略地测定周围环境中的SO2含量,某课外活动小组设计了如下图的实验装置.
(1)检查装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端浸没在水中),然后向外轻轻拉动注射器的活塞时,将会看到______ (填写实验现象),则证明该装置的气密性良好.
(2)已知二氧化硫与碘水的反应为:SO2+I2+2H2O═H2SO4+2HI.向试管中加入1.0mL溶质质量分数为1.27×10-4的碘水( 此时溶液的密度与水的密度近似 ),用适量的蒸馏水稀释后再加入2~3滴无色淀粉溶液(遇到碘单质变蓝色),配制成溶液A.测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由______色变为______色时反应恰好完全进行.
(3)课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,分别测量化学实验室和教室的空气中的S02含量.当反应恰好完全进行,记录抽气次数如下(假设每次抽气500mL).请将表二填写完整(计算时保留二位有效数字).(I-127 S-32 O-16)
表二 不同组别的测量值
(4)通过测定并计算,你判断出所测化学实验室的空气中S02的含量属于______标准(填表一中所列举的等级).

| S02最高浓度限值 | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
(1)检查装置的气密性时,先在试管中装入适量的水(保证玻璃导管的下端浸没在水中),然后向外轻轻拉动注射器的活塞时,将会看到______ (填写实验现象),则证明该装置的气密性良好.
(2)已知二氧化硫与碘水的反应为:SO2+I2+2H2O═H2SO4+2HI.向试管中加入1.0mL溶质质量分数为1.27×10-4的碘水( 此时溶液的密度与水的密度近似 ),用适量的蒸馏水稀释后再加入2~3滴无色淀粉溶液(遇到碘单质变蓝色),配制成溶液A.测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由______色变为______色时反应恰好完全进行.
(3)课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,分别测量化学实验室和教室的空气中的S02含量.当反应恰好完全进行,记录抽气次数如下(假设每次抽气500mL).请将表二填写完整(计算时保留二位有效数字).(I-127 S-32 O-16)
表二 不同组别的测量值
| 组 别 | 第一小组(实验室) | 第二小组(教室) |
| 抽气次数 | 110 | 150 |
| 空气中S02的含量 |
 人通过肺与外界进行气体交换,吸入空气,排出二氧化碳.但人体排出的二氧化碳究竟是来自空气呢,还是人体代谢作用产生的呢?某学校学生课外活动小组设计了如图所示装置进行探究.
人通过肺与外界进行气体交换,吸入空气,排出二氧化碳.但人体排出的二氧化碳究竟是来自空气呢,还是人体代谢作用产生的呢?某学校学生课外活动小组设计了如图所示装置进行探究.