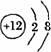题目内容
下列粒子:①分子②原子③电子④原子核⑤质子⑥中子⑦离子,带正电的是 ,带负电的是 ,不显电性的是 -,能直接构成物质的是 ,质量最小的是 ,在同一原子中数目相等的是 。
【答案】
④⑤ ③ ①②⑥ ①②⑦ ③ ③⑤
【解析】
试题分析:质子带正电,原子核带正电;由此可知:带正电的粒子是:④⑤;原子是由带正电原子核和核外带负电的电子构成,由于原子核所带正电荷数和核外电子所带负电荷数相等,电性相反,原子不显电性,分子由原子构成,分子也不显电性.故不显电性的是分子、原子、中子;分子、原子、离子都是构成物质的基本微粒;故能直接构成物质的是分子、原子、离子;原子质量主要集中在原子核上,电子质量很小,可忽略不计.在同一原子中质子数等于核电荷数等于核外电子数
考点:原子的定义与构成;分子、原子、离子、元素与物质之间的关系.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目