题目内容
【题目】用化学用语填空
(1)2个铜原子_____;(2)2个氢氧根离子_____;(3)二氧化氮_____;(4)正二价的钡元素_____;
【答案】2Cu 2OH- NO2 ![]()
【解析】
(1)原子的表示方法是用元素符号来表示一个原子,表示多个该原子,在其元素符号前加上相应的数字。 2个铜原子表示为:2Cu;
(2)离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,在其离子符号前加上相应的数字。2个氢氧根离子可表示为:2OH-;
(3)二氧化氮的化学式为:NO2;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,正二价的钡元素,故可表示为:![]() 。
。

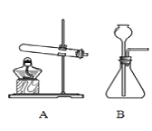
【题目】根据图中实验装置,回答问题:
发生装置 | 收集装置 | 洗气装置 |
|
|
|
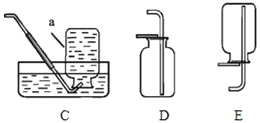
(1)仪器a的名称是__.
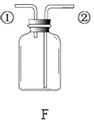
(2)实验室用高锰酸钾制取氧气,装置A还需做的改进是__________;实验室用过氧化氢溶液制取氧气,可用的发生装置是_______(选字母,下同);若用F装置收集二氧化碳,则气体应从F装置的___(填“①”或“②”)端口通入;检验CO2的化学方程式为___________。
(3)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水,可用加热氯化铵和氢氧化钙的固体混合物制取。如果要制取氨气你应选择的发生装置是___________和收集装置是________。
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)如下图是氧、硫、氯三种元素的原子结构示意图。

①氯原子的结构示意图中x的数值是_____;其在化学反应中易_______电子(填“得到”或“失去”),其离子符号为____________。
②氧和硫两种元素最本质的区别是它们原子中的__________________不同。
③具有相似化学性质的元素是______和______(填元素符号)。
④由氧元素组成的气体单质参与反应生成了一种白色固体,符号表达式为__________________。
(2)如图为元素周期表图,请回答下列问题:
IA | 0 | ||||||||
1 | 1 H 氢1.00 | ||||||||
IIA | IIIA | IVA | VA | VIA | VIIA | ||||
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | X P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 | |
①表中磷原子的核电荷数x=_______,该元素位于元素周期表的第_____周期。
②表中具有相对稳定结构的元素是________,它属于_________元素(填金属或非金属)。
③若某种铝原子的相对原子质量为27,则它的中子数为____。它与氧元素形成的化合物的化学式为____。
【题目】根据如图所示装置回答问题:

(1)写出下列仪器的名称:①__________②__________。
(2)若用不加催化剂的方法制取氧气,选择的发生装置是______,反应的化学方程式___________;该反应的基本类型为____.若选择G装置(事先装满水)收集氧气,则氧气应从_______通入(选“a”或“b”)。
(3)实验室若用装置C制取二氧化碳,与B装置相比,其优点是:_________,实验中要节约药品,如果没有说明药品的取用量,一般应取用___________.若选用上面装置来收集二氧化碳气体,可选用的收集装置是_________。
(4)鸡蛋壳的主要成分是碳酸钙.为了测定某鸡蛋壳中碳酸钙的质量分数,兴趣小组的同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取6g样品放在烧杯里(烧杯质量为10g),然后将50g稀盐酸分5次加入,每次加入稀盐酸后,用玻璃棒不断搅拌,搅拌的目的是________,充分反应后,对烧杯(包括溶液和残余固体)进行了称量(假设二氧化碳气体完全逸出,杂质不与盐酸反应),记录如下表。分析数据,进行计算:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的总质量(g) | 10 | 20 | 30 | 40 | 50 |
烧杯和药品总质量(g) | 25.56 | 35.12 | M | 54.24 | 64.24 |
M=___________g.
②鸡蛋壳样品中碳酸钙的质量分数是多少_______?(计算结果精确到0.1 %)