题目内容
【题目】工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示,下列有关甲醇的叙述中,错误的是( ) 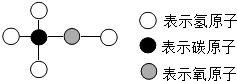
A.甲醇中C,H,O三种元素的质量比为1:4:1
B.甲醇的相对分子质量为32
C.甲醇的化学式为CH4O
D.甲醇中氧元素的质量分数为50%
【答案】A
【解析】解:根据图中的信息可知其化学式的为CH3OH,也可以写成CH4O.
A、CH4O中碳氢氧三种元素的质量比等于(12×1):(1×4):(16×1)=3:1:4,故A错误;
B、甲醇的相对分子质量等于12×1+1×4+16×1=32,故B正确;
C、物质的化学式从图中分析,体现元素组成和原子个数比例即可,不一定是对应出结构式来.图中的一个分子中有一个碳原子,四个氢原子和一个氧原子,所以其化学式为CH4O.由于碳原子是与三个氢原子和一个氧原子相连,另一氢原子是与氧原子相连的,所以也可以写成CH3OH,故C正确;
D、物质中某种元素的质量分数= ![]() ×100%.所以甲醇中氧元素的质量分数=
×100%.所以甲醇中氧元素的质量分数= ![]() ×100%=50%,故D正确.
×100%=50%,故D正确.
故选:A.
根据图中的信息可知其化学式的为CH3OH,也可以写成CH4O.之后根据化学式的意义进行分析判断即可.
A、元素的质量比等于相对原子质量与原子个数的乘积的比值,由于不同元素的相对原子质量不同,所以质量比一定不等于原子个数之比.
B、相对分子质量等于相对原子质量与原子个数的乘积的总和.
C、物质的化学式从图中分析,体现元素组成和原子个数比例即可,不一定是对应出结构式来.
D、物质中某种元素的质量分数= ![]() ×100%.
×100%.

练习册系列答案
相关题目