题目内容
【题目】等质量的a和b两种金属(已知: a和b在生成物中的化合价均为+2价)分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如下图所示。下列说法中正确的个数是
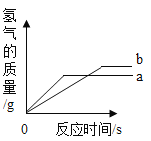
①金属a 一定可以把金属b从它的化合物溶液中置换出来
②金属b所消耗盐酸的量一定比金属a多
③反应所放出的氢气的量:金属b一定大于金属a
④相对原子质量:金属b一定大于金属a
⑤若金属b是铁,则金属a可能是锌
A.2个
B.3个
C.4个
D.5个
【答案】C
【解析】
等质量的a和b两种金属(已知: a和b在生成物中的化合价均为+2价)分别和足量的同体积、同浓度的盐酸反应,a和盐酸反应较快,则a的金属性比b强。
①由产生气体的质量与时间的关系图可知,盐酸和金属a反应生成氢气快,金属活动性顺序是a>b,金属a一定可以把金属b从它的化合物溶液中置换出来,故正确;
②金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,生成的氢气与消耗的酸的多少顺序一致,消耗盐酸的质量关系为b>a,金属b所消耗盐酸的量一定比金属a多,故正确;
③根据反应生成H2的质量与反应时间的关系图可知,在两种金属完全反应后,放出H2的质量是b>a,反应所放出的氢气的量:金属b一定大于金属a,故正确;
④a、b金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小,根据反应生成H2的质量与反应时间的关系图可知,在金属完全反应后,放出H2的质量是b>a,相对原子质量是a>b,故不正确;
⑤在金属完全反应后,放出H2的质量是b>a,相对原子质量是a>b,铁的相对原子质量为56,锌的相对原子质量为65,锌的相对原子质量大于铁,故正确。
故选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
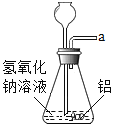
小学生10分钟应用题系列答案【题目】老师利用图示装置进行甲、乙对比实验,探究温度对一氧化碳还原氧化铁反应的影响.
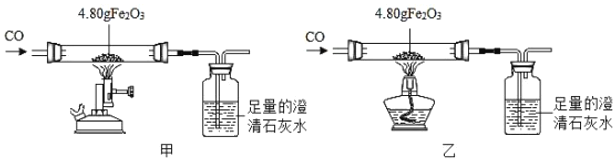
(1)从实验安全和环保角度考虑,图示装置还应采取的改进措施是_____.
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 称量黑色粉末质量/g | m1 | m2 |
2 | 取黑色粉末,用磁铁吸引 | 能被吸引 | 能被吸引 |
3 | 取黑色粉末,加入稀盐酸 | 全部溶解,有大量气泡 | 全部溶解,无气泡 |
4 | 取黑色粉末,加入足量硫酸铜溶液 | 有红色物质产生 | 无明显现象 |
①小雨同学查阅资料后发现四氧化三铁能被磁铁吸引、在常温与稀盐酸反应无气体产生、与硫酸铜溶液不反应,故猜想乙组的生成物为四氧化三铁.他又发现m2恰好为_____g(结果保留至0.01g),这可成为支持上述猜想的新证据.甲乙两组实验说明温度对一氧化碳和氧化铁反应有影响。
②若乙组的澄清石灰水变浑浊,写出乙组玻璃管内发生反应的化学方程式_____。
(3)在前面的学习中,出现过反应物种类相同,但_____不同而导致反应产物不同的情况,请举例说明_____.