题目内容
在化工生产中,有一种物质叫硫酸铈铵的常用化学试剂,其化学式为Ce(SO4)2?2(NH4)2SO4,S的化合价为+6,那么Ce的化合价是( )
| A、+2 | B、+4 | C、+5 | D、+6 |
考点:有关元素化合价的计算
专题:化学式的计算
分析:利用常见元素或原子团的化合价及化合物中元素的正负化合价的代数和为0来解答.
解答:解:根据在化合物中正负化合价代数和为零,已知铵根的化合价为+1、硫酸根为-2价;
设硫酸铈铵中Ce的化合价为x,则x+(-2)×2+2×(+1)×2+(-2)×2=0,解得x=+4;
故选:B.
设硫酸铈铵中Ce的化合价为x,则x+(-2)×2+2×(+1)×2+(-2)×2=0,解得x=+4;
故选:B.
点评:在根据化学式计算元素的化合价时,通常把原子团看作一个原子利用该原子团的化合价进行计算.

练习册系列答案
相关题目
下列有关实验现象的描述中错误的是( )
| A、木炭在氧气中燃烧,发出白光,产生的气体能使澄清石灰水变浑浊 |
| B、铁丝在空气中燃烧,火星四射,放出大量热生成黑色固体 |
| C、硫在氧气中燃烧产生耀眼的白光,放出大量热生成白色固体 |
| D、蜡烛在氧气中燃烧,发出白光,放出热量,瓶壁上有水雾,产生的气体能使澄清石灰水变浑浊 |
镧(La)(音:lán)元素在元素周期表中的原子序数为57,下列有关镧元素的说法不正确的是( )
| A、该元素原子的质子数为57 |
| B、该元素原子的核电荷数为57 |
| C、该元素原子的核外电子数为57 |
| D、该元素原子的相对原子质量为139g |
以下说法正确的是( )
| A、中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 |
| B、氧化物中含有氧元素,而含氧元素的化合物不一定是氧化物 |
| C、碱中都含有氢元素,所以含有氢元素的化合物一定是碱 |
| D、复分解反应一定有两种化合物生成,所以有两种化合物生成的反应一定是复分解反应 |
下列一氧化碳的性质中,属于化学性质的是( )
| A、可以燃烧 |
| B、难溶于水 |
| C、没有气味 |
| D、常温下为无色气体 |
下列仪器中,能在酒精灯火焰上直接加热的是( )
| A、烧杯 | B、试管 | C、集气瓶 | D、量筒 |

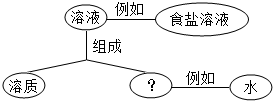 概念图能清晰地反映概念之间的联系,如图所示溶液中部分概念的相互联系,请回答:
概念图能清晰地反映概念之间的联系,如图所示溶液中部分概念的相互联系,请回答: