题目内容
【题目】学习氢氧化钠化学性质时,某化学兴趣小组设计以下实验,探究氢氧化钠与二氧化碳是否发生反应及所得溶液的溶质成分。
①从反应物减少角度探究氢氧化钠与二氧化碳是否反应。
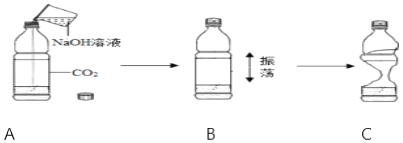
实验操作如图所示,观察到软塑料瓶变瘪,认为氢氧化钠与二氧化碳反应了,反应的化学方程式为_____;一位同学认为此实验操作及现象不足以证明氢氧化钠与二氧化碳发生了反应,其理由是_____;小组同学进一步思考讨论后,他们用和甲相同的充满二氧化碳的软塑料瓶,加入_____,做了对照实验,完善了方案。
②从生成物角度探究氢氧化钠与二氧化碳是否反应,取上述方案C中的溶液少许,滴加_____,观察到有产生气泡,证明氢氧化钠与二氧化碳发生了反应。
③探究方案①中C的溶质成分
实验步骤 | 实验现象 | 实验结论 |
步骤一:取少量样品,滴加___________ | 产生白色沉淀 | 溶质成分为_____ |
步骤二:_____ | _____ |
【答案】 CO2+2NaOH=Na2CO3+H2O 二氧化碳能溶于水且能与水反应生成碳酸 略 滴加足量(过量)稀盐酸 足量(过量)氯化钡溶液 取步骤一上层清液,滴加无色酚酞试液 溶液变为红色 碳酸钠、氢氧化钠;
【解析】(1)氢氧化钠与二氧化碳反应生成碳酸钠和水,反应方程式为CO2+2NaOH=Na2CO3+H2O;瓶子变瘪是由于二氧化碳的含量减少而引起,二氧化碳减少可能是由于二氧化碳与氢氧化钠反应而减少,也可能是由于二氧化碳溶于水而减少,故不能确定二氧化碳与氢氧化钠一定发生了反应;将等体积的氢氧化钠溶液和水进行对比实验,发现装有氢氧化钠的瓶子变瘪的程度较大,说明二氧化碳与氢氧化钠发生了反应;
(2)如氢氧化钠与二氧化碳发生了反应,则生成了碳酸钠和水,故可以加入过量的稀盐酸,如有气泡冒出,说明有碳酸钠生成,从而说明二氧化碳与氢氧化钠发生了反应;
(3)丙中的溶质可能是碳酸钠与氢氧化钠的混合物,故向溶液中加入过量的氯化钡溶液,有白色沉淀生成,说明有碳酸钠,在取上清液加入酚酞,溶液变为红色,说明有氢氧化钠,最终得出,溶液中有碳酸钠和氢氧化钠;

 名题金卷系列答案
名题金卷系列答案【题目】如图是一套检验气体性质的实验装置,向装置中持续通入气体X,若打开活塞K,只观察到紫色石蕊变红;若关闭活塞K,可观察到紫色石蕊试液变红,澄清石灰水变浑浊。据此判断气体X和洗瓶内的液体Y可能是( )
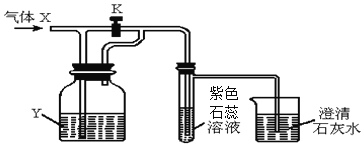
A | B | C | D | |
X | 二氧化碳 | 氯化氢 | 二氧化碳 | 氯化氢 |
Y(足量) | 水 | 碳酸钠溶液 | 氢氧化钠溶液 | 氢氧化钠溶液 |
A. A B. B C. C D. D