题目内容
【题目】某科研小组设计利用稀硫酸浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反应,也不溶解于水)的方案,实现废物综合利用。部分实验流程如图:
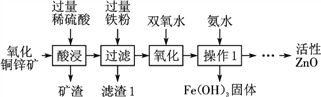
请根据上述实验流程回答下列问题:
(1) 操作1的名称是________。
(2) 在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为__________________________(任写一个)
(3) 加过量铁粉后,发生反应的基本反应类型是______,得到滤渣1的成分为_______(填化学式)。
(4) 在实验过程中,双氧水会与Fe2+反应生成Fe3+和水,以便在后续的操作中将溶液中铁元素除去。高锰酸钾溶液也能将Fe2+氧化成Fe3+,选用双氧水的优点是____________________________。
【答案】 过滤 CuO+H2SO4═CuSO4+H2O,ZnO+H2SO4═ZnSO4+H2O 置换反应 Fe、Cu 不引人较难除去的杂质
【解析】(1) 操作1的名称是过滤,过滤能把沉淀和滤液分开;(2)在氧化铜锌矿中加入过量稀硫酸,稀硫酸和氧化铜反应生成硫酸铜和水,和氧化锌反应生成硫酸锌和水,反应的化学方程式为:CuO+H2SO4═CuSO4+H2O或ZnO+H2SO4═ZnSO4+H2O;(3)加过量铁粉后,铁和稀硫酸反应生成硫酸亚铁和氢气,和硫酸铜反应生成氯化亚铁和铜,发生反应的基本反应类型是置换反应,得到滤渣1的成分是反应生成的铜和过量的铁,故填:Cu、Fe;(4)在实验过程中,选用双氧水的优点是过氧化氢被还原成水,不带入新的杂质。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】化学家用![]() 与
与![]() 在高温高压、催化剂的作用下,制得了纳米级别的金刚石,同时得到一种白色固体。白色固体是什么呢?同学们对这个问题产生了兴趣,并进行了下面探究:
在高温高压、催化剂的作用下,制得了纳米级别的金刚石,同时得到一种白色固体。白色固体是什么呢?同学们对这个问题产生了兴趣,并进行了下面探究:
【提出问题】白色固体的成分是什么?
【查阅资料】
碳酸钠、氧化钠![]() 均为白色固体。
均为白色固体。
氧化钠与水在常温下反应生成氢氧化钠,化学方程式为: ![]() 。
。
③![]() 溶液呈中性,
溶液呈中性, ![]() 是不溶于水的白色固体。
是不溶于水的白色固体。
【提出猜想】甲同学:白色固体是氧化钠;乙同学:白色固体是碳酸钠;丙同学:白色固体是氧化钠和碳酸钠的混合物。
【实验与结论】
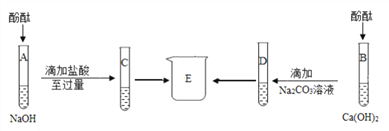
(1)甲同学为验证猜想,取白色固体样品于试管中,加适量水,滴加无色酚酞溶液,观察到酚酞溶液变红,于是得出自己的猜想正确,但遭到其他同学反对,原因是_______________。
乙、丙两位同学设计了以下方案进行验证:
实验步骤 | 实验现象 | 实验结论 |
①取少量白色固体样品于试管中,加入足量水将其溶解,并加入过量的______ | 试管中产生白色沉淀 | 白色固体中有碳酸钠 |
②往实验①反应后的试管中滴加____ | _______ | 白色固体中没有氧化钠 |
通过上述实验可证明乙同学的猜想正确,请写出金属钠与二氧化碳反应的化学方程式:_____ 。
【拓展延伸】蜡烛火焰中也含有金刚石,碳转化为金刚石的微观本质是___________。