题目内容
【题目】该兴趣小组同学为了测定变质的烧碱样品中Na2CO3的质量分数.(碱石灰是CaO与NaOH的固体混合物) 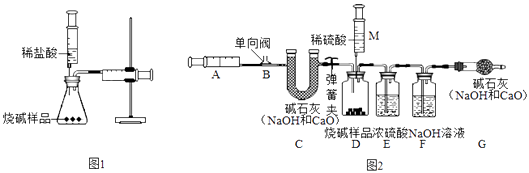
(1)首先设计了图1所示的装置,加入过量的盐酸反应后,通过右侧注射器内收集到气体的量计算出Na2CO3的质量分数(所使用注射器最大量程为20mL).写出锥形瓶内所发生变化的化学方程式(写一个即可 .
小李认为该方案中需要控制样品取用的量,这是因为 .
(2)该兴趣小组同学在反思上面实验后设计了如图2的装置测定变质的烧碱样品中Na2CO3的质量分数.反应的开始、结束都要用注射器反复的排送空气.
实验步骤为:
①检查装置的气密性.
②称10g烧碱样品放入广口瓶中,D处注射器内加入适量的稀硫酸,准确称量装置F的质量320g,连好装置.
③打开弹簧夹,反复推拉注射器A10次,准确称量装置F的质量320.5g.
④关闭弹簧夹,然后推动注射器M的活塞,让稀硫酸逐滴滴入样品中,直到不再产生气泡为止.
⑤打开弹簧夹,缓缓推拉注射器A10次.
⑥再准确称装置F质量为321.6g.
问题探究:
(Ⅰ)图2中E装置的作用是 .
(Ⅱ)若步骤⑤中注射器A推拉速率过快,则测定的Na2CO3的质量分数会(填“偏大”、“偏小”、“不变”),理由是 .
【答案】
(1)NaOH+HCl═NaCl+H2O或Na2CO3+2HCl═2NaCl+H2O+CO2↑;若样品取多了,产生气体可能超过注射器量程,若样品取少了,产生气体太少,无法测量
(2)吸收进入F装置气体中的水蒸气;偏小;生成二氧化碳气体不能完全被NaOH溶液吸收
【解析】解:(1)已知“某变质的烧碱样品中有Na2CO3”,所以和盐酸反应的化学方程式应有两个,及氢氧化钠和碳酸钠与盐酸的反应,反应的方程式分别为:NaOH+HCl=NaCl+H2O;Na2CO3+2HCl=2NaCl+H2O+CO2↑; 由题意可知,所使用注射器最大量程为20mL,若样品取多了,产生气体可能超过注射器量程,若样品取少了,产生气体太少,无法测量,因此需要控制样品取用的量;(2)(Ⅰ)浓硫酸具有吸水性,图2中E装置的作用是吸收进入F装置气体中的水蒸气.(Ⅱ)若二氧化碳释放的太快,不能被氢氧化钠完全吸收,会使测定的Na2CO3的质量分数偏小;
故答为:(1)NaOH+HCl═NaCl+H2O 或Na2CO3+2HCl═2NaCl+H2O+CO2↑;若样品取多了,产生气体可能超过注射器量程,若样品取少了,产生气体太少,无法测量.(2)(Ⅰ)吸收进入F装置气体中的水蒸气;(Ⅱ)偏小;理由是:生成二氧化碳气体不能完全被NaOH溶液吸收.
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.