题目内容
【题目】为测定鸡蛋壳中碳酸钙的含量(杂质不溶于水,也不与稀盐酸反应),某小组同学将鸡蛋壳清洗干净,晾干,取15g鸡蛋壳研碎,逐滴加入稀盐酸,当加入94.4g稀盐酸时恰好完全反应,反应产生的二氧化碳用足量的氢氧化钠溶液吸收,实验中氢氧化钠溶液的质量变化如图所示。

请计算:
(1)生成二氧化碳的质量为______ g。
(2)计算鸡蛋壳中碳酸钙的质量。______(写出计算过程)
(3)计算反应后所得溶液的溶质质量分数。______(写出计算过程)
【答案】4.4 10g 11.1%
【解析】
(1)生成二氧化碳的质量为54.4g-50g=4.4g,
故填:4.4。
(2)设鸡蛋壳中碳酸钙的质量为x,反应生成氯化钙质量为y,
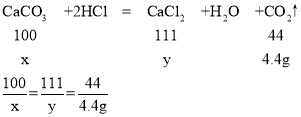
x=10g,y=11.1g,
答:碳酸钙质量是10g。
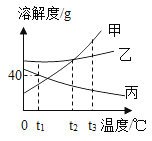
(3)反应后所得溶液的溶质质量分数为:![]() ×100%=11.1%,
×100%=11.1%,
答:反应后所得溶液的溶质质量分数为11.1%。

【题目】钠是一种活泼金属,常温下能与氧气、水等物质发生反应。钠与水反应的化学方程式为:2Na+2H2O==2NaOH+H2↑。在实验室,小亮先取定量的硫酸铜溶液于烧杯中,再取一小块钠投入硫酸铜溶液中,充分反应后过滤,得到滤液和蓝色滤渣,并对滤被的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(查阅资料)Na2SO4溶液呈中性
(猜想与假设)猜想一:Na2SO4
猜想二:Na2SO4和NaOH
猜想三:____________
猜想四:Na2SO4、CuSO4和NaOH
小明认为猜想______不合理,理由是_______(用化学方程式表示)。
(实验与验证)
实验 | 实验操作 | 实验現象 | 实验结论 |
实验一 | 取少量滤液于试管中,仔细观察现象 | 溶液为无色 | 猜想_____不成立 |
实验二 | 向实验一所取滤液中滴入酚酞溶液 | ________ | 猜想二不成立 |
实验三 | 常温下,再取少量滤液,测溶液酸碱度 | pH=7 | 猜想_____成立 |
(拓展延伸)金属活动性顺序表中钠及前面的金属____(填“能”或“不能”)把位于后面的金属从它们盐溶液里置换出来。