题目内容
【题目】盐酸是一种重要的化工产品,也是实验室中重要的化学试剂,用途广泛. 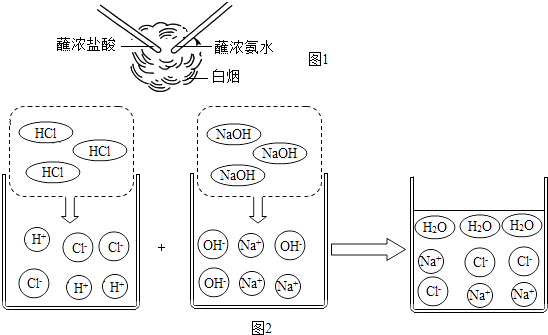
(1)增大压强,HCl由气态为液态,从微观的角度分析该变化过程中改变的是 .
(2)蘸浓盐酸的玻璃棒和蘸浓氨水的玻璃棒接近但不接触,发生了如图1的现象,反应的化学方程式是 , 浓盐酸和浓氨水都具有挥发性,气体有刺激性和腐蚀性,实验时要注意 .
(3)观察图2并回答问题: 由图2可知,HCl和NaOH的反应实质是H+和OH﹣之间的反应,此反应可表示为:H++0H﹣=H2O.像这种用实际参与反应的离子来表示反应的式子称为离子方程式.任何复分解反应都可用离子方程式来表示.
【练习】按照书写化学方程式的要求写出下列反应的离子方程式
HCl溶液与AgNO溶液反应: .
HNO3溶液与Na2CO3溶液反应: .
【归纳】复分解反应的实质是:阴阳离子结合生成的反应.
【应用】判断在水溶液中一定能大量共存的离子组是 .
A.Na+、H+、Cl﹣、CO32﹣ B.H+、Ba2+、Cl﹣、SO42﹣
C.Cu2+、Na+、NO3﹣、OH﹣ D.H+、K+、Cl﹣、SO42﹣ .
【答案】
(1)氯化氢分子之间的间隔变小
(2)NH3+HCl=NH4Cl;在通风厨中进行
(3)Ag++Cl﹣=AgCl;2H++CO32﹣=H2O+CO2↑;水、沉淀、气体;D
【解析】解:(1)增大压强,HCl由气态为液态,从微观的角度分析该变化过程中改变的是氯化氢分子之间的间隔变小. 故填:氯化氢分子之间的间隔变小.(2)氨气和氯化氢反应的化学方程式是:NH3+HCl=NH4Cl,浓盐酸和浓氨水都具有挥发性,气体有刺激性和腐蚀性,实验时要注意在通风厨中进行.
故填:NH3+HCl=NH4Cl;在通风厨中进行.(3)HCl溶液与AgNO溶液反应的离子方程式为:Ag++Cl﹣=AgCl.
故填:Ag++Cl﹣=AgCl.
HNO3溶液与Na2CO3溶液反应的离子方程式为:2H++CO32﹣=H2O+CO2↑.
故填:2H++CO32﹣=H2O+CO2↑.
复分解反应的实质是:阴阳离子结合生成水、沉淀、气体的反应.
故填:水、沉淀、气体.
A、氢离子和碳酸根离子结合生成水和二氧化碳,因此该选项离子不能共存;
B、钡离子能和硫酸根离子结合成硫酸钡沉淀,因此该选项不能共存;
C、铜离子和氢氧根离子结合成氢氧化铜沉淀,因此该选项不能共存;
D、离子之间不能反应,因此该选项能够共存.
故填:D.
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号,以及对分子的定义与分子的特性的理解,了解分子是保持物质化学性质最小的微粒;性质:体积小、质量小;不断运动;有间隙.





