题目内容
【题目】(6分)蕲春实验中学化学兴趣小组,在学习碱的化学性质时,进行了如图1所示的实验。
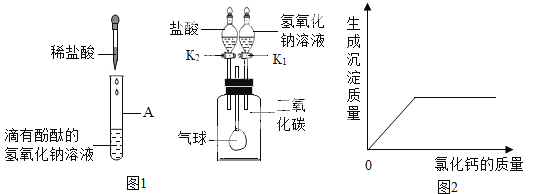
(1)第一组同学在向A中加入一定量的稀盐酸后,发现A中溶液仍然呈红色,则反应后溶液中的溶质是(酚酞除外,用化学式表示) ;第二组同学做完A实验后溶液呈无色,用微观理论解释A中溶液变为无色的反应的实质是 。
(2)第三组同学做B实验用于确认二氧化碳与氢氧化钠能发生化学反应(实验前K1、K2均处于关闭状态)。B实验全过程的操作及现象是:
步骤 | 现象 |
第一步: ; | 气球胀大 |
第二步: 。 | 气球又缩小至原来状态 |
(3)请写出气球缩小至原来状态的化学方程式 。
(4)实验结束后,小军将以上同学做的A、B两个实验的废液均倒入同一个大烧杯中,观察到混合后的废液呈红色,由此产生疑问:
[提出问题]大烧杯的废液中含有哪些溶质?(酚酞除外)
[查阅资料]氯化钙溶液呈中性,CaCl2+Na2CO3=CaCO3↓+2NaCl
[实验验证]取一定量的废液,逐滴加入氯化钙溶液,如图2为同学们根据部分实验现象绘制的关系曲线。
[实验结论]如果观察到的现象只有沉淀产生,溶液仍然为红色,则废液中的溶质为 ;如果观察到有沉淀产生,溶液仍由红色变为无色,则废液中的溶质为 。
【答案】 (1)NaOH、NaCl 氢氧化钠溶液中的氢氧根离子与稀盐酸中的氢氧根离子反应生成了水分子 (2)打开K1,关闭K2 打开K2,关闭K1 (3)Na2CO3+2HCl=2NaCl+H2O+CO2↑ (4)NaOH、Na2CO3、NaCl Na2CO3、NaCl
【解析】
试题分析: 酸碱发生中和反应,溶液仍然呈现红色说明碱没有反应完,故(1)第一组同学在向A中加入一定量的稀盐酸后,发现A中溶液仍然呈红色,则反应后溶液中的溶质是NaOH、NaCl;第二组同学做完A实验后溶液呈无色,说明溶液中没有聊氢氧根离子,故用微观理论解释A中溶液变为无色的反应的实质是氢氧化钠溶液中的氢氧根离子与稀盐酸中的氢氧根离子反应生成了水分子;(2)第三组同学做B实验用于确认二氧化碳与氢氧化钠能发生化学反应(实验前K1、K2均处于关闭状态)。B实验全过程的操作及现象是:根据实验现象可知操作为第一步为打开K1,关闭K2,,氢氧化钠与二氧化碳反应使气体的压强减小;第二步;打开K2,关闭K1,滴入盐酸,盐酸与生成的碳酸钠反应生成气体,使瓶内压强增大;(3)请写出气球缩小至原来状态的化学方程式,Na2CO3+2HCl=2NaCl+H2O+CO2↑,(4)实验结束后,小军将以上同学做的A、B两个实验的废液均倒入同一个大烧杯中,观察到混合后的废液呈红色,说明溶液呈碱性,[提出问题]大烧杯的废液中含有哪些溶质,实验探究, [实验结论]如果观察到的现象只有沉淀产生,溶液仍然为红色,说明溶液中既有碳酸钠还有氢氧化钠,故废液中的溶质为NaOH、Na2CO3、NaCl ;如果观察到有沉淀产生,溶液由红色变为无色,说明溶液中有碳酸钠,反应后没有碱性物质,则废液中的溶质为Na2CO3、NaCl。

 阅读快车系列答案
阅读快车系列答案【题目】(7分) 某学生做了如下图所示的实验。
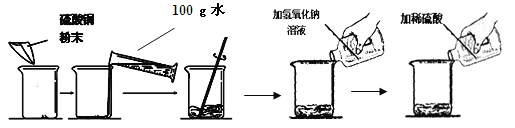
第一次 | 第二次 | |
加入硫酸铜的质量 | m | m |
加入氢氧化钠溶液的质量 | 50g(溶质质量分数16%) | 50g(溶质质量分数16%) |
加入稀硫酸的质量 | 50g | 100g |
实验现象 | 蓝色固体和蓝色溶液 | 蓝色溶液 |
若第二次所加物质恰好完全反应(溶液损失忽略不计),请回答下列问题:
(1)写出实验中发生反应的化学方程式___________________________;
(2)第一次实验后的溶液中所含溶质的化学式为___________________________;
(3)根据已知条件列出求解实验中生成沉淀的质量(x)的比例式______;
(4)实验中加入硫酸铜的质量(m)为______;
(5)在第二次实验中,若向加入氢氧化钠溶液反应后的滤液中加入43.8 g水,则所得溶液中溶质的质量分数为_____________;
(6)若用溶质质量分数为98%的硫酸溶液配制实验中所需的稀硫酸,则需要加水的质量为_________。