题目内容
【题目】黄铜矿经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4,利用如图实验可制取补血剂原料碳酸亚铁并回收铜。
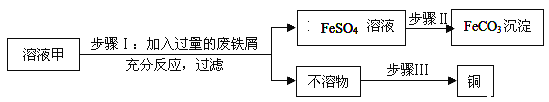
(1)步骤Ⅰ中,发生反应的化学方程式包括:
①Fe2(SO4)3+Fe![]() 3FeSO4;
3FeSO4;
②_________________________;
③_________________________。
(2)步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是_____________(填化学式)。
(3)步骤Ⅲ回收铜的实验操作包括:①过滤、②洗涤、③加足量稀硫酸、④干燥,正确的操作排序是____________(填序号)。
(4)若废铁屑含有少量铁锈,对达成实验目的______(填“有”或“无”)影响。
(5)查资料可知,Fe2+在空气中可氧化成Fe3+,为防止FeSO4溶液在空气中氧化,可在溶液中加入少量___________ 。
【答案】 Fe+H2SO4=FeSO4+H2↑ Fe+CuSO4=Cu+FeSO4 Na2CO3/K2CO3 ③①②④ 无 铁粉。
【解析】(1)Fe2(SO4)3、CuSO4及H2SO4都能与铁反应,反应的方程式为:Fe+H2SO4=FeSO4+H2↑; Fe+CuSO4=FeSO4+Cu;
(2)步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是Na2CO3,碳酸钠与硫酸亚铁反应生成碳酸亚铁沉淀;
(3)步骤Ⅲ回收铜的实验操作因不溶物中含有铜和铁,先加足量稀硫酸,与铁反应,然后过滤则不容的部分为铜,再经过洗涤、干燥得到铜;
(4)溶液中含有硫酸铜,硫酸铜和加入的铁屑反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是铁锈与硫酸反应生成硫酸铁,硫酸铁和铁会生成硫酸亚铁;
(5)FeSO4被氧化而变质,应加入具有还原性的物质,且溶液配制中不能引入新的杂质,所以加入少量的铁粉。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案